Resistencia a los antibióticos

Resistencia a los antibióticos es una forma de resistencia a los medicamentos por el que algunos (o, menos comúnmente, todas) las subpoblaciones de una microorganismo, generalmente una especie bacteriana, son capaces de sobrevivir después de la exposición a uno o más antibióticos; se consideran patógenos resistentes a múltiples antibióticos multirresistentes (MDR) o, más coloquialmente, superbacterias.[1]
Resistencia a los antibióticos es un fenómeno grave y creciente en la medicina contemporánea y ha emergido como una de las preocupaciones de salud pública preeminente del siglo XXI, en particular en lo que respecta a los organismos patógenos (el término es especialmente relevante para los organismos que causan enfermedades en los seres humanos). A Organización Mundial de la salud informe difundido el 30 de abril de 2014 Estados esta grave amenaza ya no es una predicción para el futuro, que está pasando ahora en todas las regiones del mundo y tiene el potencial de afectar a cualquier persona, de cualquier edad, en cualquier país. Resistencia a los antibióticos – cuando la bacteria cambia para los antibióticos ya no funcionan en las personas que las necesitan para tratar las infecciones – ahora es una gran amenaza para la salud pública. "[2]
En los casos más simples, los organismos resistentes a drogas hayan adquirido resistencia a los antibióticos de primera línea, lo que requiere el uso de agentes de segunda línea. Típicamente, un agente de primera línea se selecciona en base a varios factores, incluyendo seguridad, disponibilidad y costo; un agente de segunda línea es generalmente más amplio espectro, tiene un perfil de riesgo / beneficio menos favorable y es más caro o, en circunstancias extremas, puede no estar disponible localmente. En el caso de algunos patógenos MDR, resistencia a los antibióticos de segunda y hasta tercera línea es, por lo tanto, secuencialmente adquirida, esencialmente ilustrado por un caso Estafilococo áureo en algunos nosocomial Configuración. Algunos patógenos, tales como Pseudomonas aeruginosa, también poseen un alto nivel de resistencia intrínseca.
Puede tomar la forma de un espontáneo o inducido genética mutación, o la adquisición de resistencia genes de otras especies bacterianas por transferencia horizontal de genes Via Conjugación, transducción de señales, o transformación. Muchos genes de resistencia a los antibióticos residen en transmisible plásmidos, facilitando su transferencia. Exposición a un antibiótico selecciona naturalmente para la supervivencia de los organismos con los genes de resistencia. De esta manera, un gen de resistencia a los antibióticos puede extenderse fácilmente a través de un ecosistema de bacterias. Los plásmidos de resistencia a antibióticos con frecuencia contienen genes que confieren resistencia a varios antibióticos diferentes. Esto no es el caso de Tuberculosis del Mycobacterium, la bacteria que causa Tuberculosis, puesto que se carecen de pruebas para si estas bacterias tienen plásmidos.[3] También M. tuberculosis carecen de la oportunidad de interactuar con otras bacterias con el fin de compartir los plásmidos.[3][4]
Genes de resistencia a los antibióticos, como los antibióticos, son antiguos.[5] Sin embargo, la creciente prevalencia de infecciones bacterianas resistentes a los antibióticos en la práctica clínica proviene de antibiótico usar tanto en medicina humana y Medicina Veterinaria. Cualquier uso de antibióticos puede aumentar presión selectiva en una población de bacterias para permitir que las bacterias resistentes a prosperar y las bacterias susceptibles a morir. Como resistencia a los antibióticos se vuelve más común, se presenta una mayor necesidad de tratamientos alternativos. Sin embargo, a pesar de un empujón para nuevas terapias antibióticas, ha habido una disminución constante del número de medicamentos recientemente aprobados.[6] Resistencia a los antibióticos por lo tanto, plantea un problema significativo.
La creciente prevalencia e incidencia de infecciones por patógenos MDR está tipificado por el creciente número de familiares siglas utilizadas para describir el agente causativo y a veces la infección; de éstos, MRSA es probablemente la más conocida, pero otros incluyendo VISA (vancomicina-intermedio S. aureus), (Resistente a la vancomicina VRSA S. aureus), ESBL (beta-lactamasas de espectro extendido), VRE (resistente a la vancomicina Enterococo) y MRAB (Multidrug-resistant A. baumannii) son ejemplos prominentes. Infecciones nosocomiales dominan abrumadoramente casos donde están implicados agentes patógenos MDR, pero infecciones multirresistentes también se están volviendo cada vez más común en la comunidad.
Contenido
- 1 Causa
- 1.1 Ocurrencia natural
- 1.2 Medicina
- 1.3 Medicina Veterinaria
- 1.4 Estados Unidos
- 2 Impacto ambiental
- 3 Mecanismos
- 4 Patógenos resistentes
- 4.1 Estafilococo áureo
- 4.2 Estreptococo y Enterococo
- 4.3 Pseudomonas aeruginosa
- 4.4 El Clostridium difficile
- 4.5 Salmonella y E. coli
- 4.6 Acinetobacter baumannii
- 4.7 Klebsiella pneumoniae
- 4.8 Tuberculosis del Mycobacterium
- 4.9 Neisseria gonorrhoeae
- 5 Prevención
- 5.1 Recomendaciones de la organización de salud mundial
- 5.2 Prevención de infecciones
- 5.3 Terapia phage
- 6 Investigación
- 6.1 Desarrollo
- 6.2 Mecanismo
- 6.3 Aplicaciones
- 7 Véase también
- 8 Notas al pie
- 9 Referencias
- 10 Enlaces externos
Causa
Aunque hubo niveles bajos de bacterias resistentes a los antibióticos preexistentes antes del uso generalizado de antibióticos,[7] [8] la presión evolutiva de su uso ha desempeñado un papel en el desarrollo de variedades resistentes a la tuberculosis y la propagación de la resistencia entre las especies bacterianas.[9] El uso generalizado de antibióticos tanto dentro como fuera de la medicina está jugando un papel importante en la aparición de bacterias resistentes.[10]
En algunos países, los antibióticos se venden en el mostrador sin necesidad de receta, que también conduce a la creación de cepas resistentes. Incluyen otras prácticas contribuyen a la resistencia uso de antibióticos en el ganado alimentación para promover un crecimiento más rápido.[11][12] Uso doméstico de antibacterianos en jabones y otros productos, aunque no claramente contribuye a la resistencia, también se desaconseja (por no ser eficaz en el control de la infección).[13] Unsound prácticas en la industria de fabricación de productos farmacéuticos pueden contribuir también a la posibilidad de crear cepas resistentes a los antibióticos.[14] Los procedimientos y la práctica clínica durante el período de tratamiento farmacológico con frecuencia presentan defectos — generalmente no se tomaron medidas para aislar al paciente para prevenir la reinfección o infección por un patógeno nuevo, negando la meta de destrucción completa al final del curso[15] (véase Infecciones relacionadas con la salud y Control de la infección).
Ciertas clases de antibióticos se asocian más altamente con la colonización "superbacterias" comparados con otras clases de antibióticos. Una superbacteria, también llamado multirresistentes, es una bacteria que lleva varios genes de resistencia.[16] Si hay una falta de susceptibilidad (resistencia) de las superbacterias al antibiótico usado y penetración del tejido alta, así como amplio espectro de actividad contra las bacterias"buenas" aumenta el riesgo para la colonización. En el caso de MRSA, aumento de las tasas de infecciones por SARM se observan con glicopéptidos, cefalosporinasy especialmente quinolonas.[17][18] En el caso de la colonización con El Clostridium difficile, los antibióticos de alto riesgo incluyen cefalosporinas y quinolonas particulares y clindamicina.[19][20]
De los antibióticos usados en los Estados Unidos en 1997, la mitad fueron utilizada en los seres humanos y la otra mitad en animales; en 2013, el 80% fueron utilizado en los animales.[21][22]
Ocurrencia natural
Hay evidencia que naturalmente la resistencia a los antibióticos que ocurren es común.[23] El genes que conferir esta resistencia se conoce como el medio ambiente resistome.[23] Estos genes pueden transferirse de las bacterias causantes de enfermedades a aquellos que causan la enfermedad, llevando a clínicamente significativa resistencia a los antibióticos.[23]
En 1952, un experimento realizado por Joshua y Esther Lederberg demostró que penicilina-bacterias resistentes existieron antes de tratamiento con penicilina.[24] Al mismo tiempo experimentando en el Universidad de Wisconsin-MadisonJoshua Lederberg y su estudiante graduado Norton Zinder también demostraron resistencia bacteriana preexistente a estreptomicina.[25] En 1962, la presencia de penicilinasa fue detectada en latente Bacillus licheniformis endosporas, revivió de suelo seco de las raíces de las plantas, conservadas desde 1689 en el Museo Británico.[26][27][28] Seis cepas de Clostridium, encontró en las entrañas de William Braine y John Hartnell (miembros de la Expedición de Franklin) mostraron resistencia a cefoxitina y clindamicina.[29] Se sugirió que penicilinasa puede han surgido como un mecanismo de defensa para las bacterias en su hábitats, como en el caso de penicilinasa-ricos Estafilococo áureo, viviendo con la producción de penicilina Trichophyton, sin embargo esto se consideró circunstancial.[28] Búsqueda de un antepasado de penicilinasa se ha centrado en la clase de proteínas Eso debe ser a priori capaz de combinación específica con penicilina.[30] La resistencia a este medicamento y clindamicina a su vez fue atribuida a de Braine y de Hartnell contacto con los microorganismos que las producen naturalmente o mutación aleatoria En cromosomas de Clostridium cepas.[29] Sin embargo, hay evidencia de que metales pesados y algunos contaminantes pueden seleccionar para las bacterias resistentes a los antibióticos, generando una fuente constante de ellos en pequeñas cantidades.[31]
Medicina
El volumen de antibiótico prescrito es el principal factor en el aumento de tarifas o resistencia bacteriana en lugar de conformidad con los antibióticos.[32] Prescripción inapropiada de antibióticos ha sido atribuida a varias causas, incluidas las personas insisten en antibióticos, los médicos prescribirlos que sienten que no tienen tiempo para explicar por qué no son necesarios y los médicos no saber cuándo prescribir antibióticos o excesivamente cauteloso por razones médicas o legales.[33] Por ejemplo, un tercio de las personas creen que los antibióticos son efectivos para el resfriado común,[34] y el resfriado común es que los antibióticos mas comunes de la razón se instalan los[35] Aunque los antibióticos son inútiles contra los virus. Un solo régimen de antibióticos incluso en pacientes compatibles con conduce a un mayor riesgo de organismos resistentes a ese antibiótico en persona durante un mes y posiblemente un año.[36]
Resistencia a los antibióticos se ha demostrado que aumentan con la duración del tratamiento; por lo tanto, mientras se observa un límite inferior eficaz, el uso por la comunidad médica de cursos cortos de antibióticos es probable a disminuir las tasas de resistencia, reducir costos y tener mejores resultados debido a menos complicaciones tales como C. difficile infección y diarrea.[37][38][39][40][41][42][43][44] En algunas situaciones un curso corto es inferior a un curso largo.[45]
A BMJ editorial recomienda que los antibióticos pueden ser a menudo salvo detenidos 72 horas después de que los síntomas se resuelven.[46] Porque los pacientes pueden sentir mejores antes de que la infección sea erradicada, médicos deben proporcionar instrucciones a los pacientes para que sepan cuándo es seguro que deje de tomar una receta. Algunos investigadores abogan por médicos usando un curso muy corto de antibióticos, reevaluar al paciente después de unos días y suspender el tratamiento si ya no hay signos clínicos de infección.[47]
Los pacientes que toman menos de la dosis requerida o en su defecto tomar sus dosis dentro de los resultados en el tiempo prescrito disminuyó la concentración de antibióticos en la sangre y los tejidos, y, a su vez, la exposición de bacterias a concentraciones de antibióticas subóptimas aumenta la frecuencia de organismos resistentes a los antibióticos, sin embargo los factores dentro de la configuración de la unidad de cuidados intensivos como la ventilación mecánica y múltiples enfermedades subyacentes también aparecieron contribuir a la resistencia bacteriana.[48] Estos pacientes de neumonía nosocomial representan una situación donde hubo relativamente poco aporte de defensa del huésped al resultado, y por lo tanto, pueden no ser aplicable a sanas individuos tomando antibióticos.
Higiene de las manos pobres por personal del hospital se ha asociado con la propagación de organismos resistentes,[49] y un aumento en la mano que se lava cumplimiento de resultados en las tasas de disminución de estos organismos.[50]
El uso inapropiado de antibióticos y tratamientos terapéuticos a menudo se puede atribuir a la presencia de violencia estructural en determinadas regiones. Factores socioeconómicos como la raza y la pobreza afectan a la accesibilidad de y la adherencia al tratamiento farmacológico. La eficacia de los programas de tratamiento para estas cepas farmacorresistentes depende o no mejoras programáticas toman en cuenta los efectos de la violencia estructural.[51]
Medicina Veterinaria
La aparición de microorganismos resistentes a los antibióticos en medicina humana es principalmente el resultado de la utilización de antibióticos en los seres humanos, aunque el uso de antibióticos en los animales también es en parte responsable.[52]
Desde el último tercio del siglo XX, ha habido un uso extensivo de los antibióticos en cría de animales. Algunas de estas drogas no se consideran significativos para su uso en seres humanos, debido a su falta de eficacia o de propósito en los seres humanos (como el uso de ionopores en rumiantes[53]), o porque esa droga ha salido en su mayoría de uso en seres humanos (tales como sulfonamidas debido a las reacciones alérgicas generalizadas y resistencia a los antibióticos entre patógenos humanos)[citación necesitada]. Otros sin embargo se utilizan en animales y seres humanos, como la penicilina y algunas formas de tetraciclina.[54] Históricamente, la regulación del uso de antibióticos en los animales de alimentos se ha limitado a limitar los residuos de droga en carne, huevos y productos lácteos, en lugar de interés directo sobre el desarrollo de resistencia a los antibióticos. Esto refleja las preocupaciones principales en la medicina humana, donde, en general, los investigadores y médicos estaban más preocupados por las dosis eficaces pero no tóxicos de las drogas en lugar de resistencia a los antibióticos.
Las bacterias resistentes que exposición antibiótica selecciona en animales pueden ser transmitidas a los humanos a través de tres vías, a través del consumo de los productos de origen animal (leche, carne, huevos, etc.), por el contacto cercano o directo con animales o con otros seres humanos, o a través del entorno.[55] En la primera vía, conservación de alimentos los métodos pueden ayudar a eliminar, reducir o prevenir el crecimiento de bacterias en algunas clases de alimentos. Pruebas para la transferencia de microorganismos resistentes a antibióticos de los animales a los seres humanos han sido escasos, y la mayoría demuestra que los patógenos de importancia en las poblaciones humanas se originaron en los seres humanos y se mantienen allí, con raros casos de transferencia a los seres humanos.[56][57] El uso de antibióticos en los animales puede clasificarse en patrones de uso diferentes según su propósito. La clasificación más aceptada discrimina terapéutica, profiláctica, metaphylactic y promoción del crecimiento, usa de antibióticos.[58] Todos los cuatro patrones Seleccione para resistencia bacteriana, ya que la resistencia a los antibióticos es un proceso evolutivo natural, pero los usos no terapéuticos exponen un número más grande de los animales y por lo tanto de bacterias, por más largos períodos y en dosis más bajas. Por lo tanto aumentan grandemente la sección representativa de la evolución de la resistencia.
El Organización Mundial de la salud concluyó que el uso inadecuado de antibióticos en la ganadería es un contribuyente subyacente a la aparición y la propagación de gérmenes resistentes a los antibióticos, y que alimenta el uso de antibióticos como promotores del crecimiento en animales debe prohibirse, en la ausencia de evaluaciones de riesgo. Con respecto a este asunto, el OIE ha añadido que el código de salud de animales terrestres una serie de directrices con recomendaciones a sus miembros para la creación y armonización de la vigilancia de la resistencia antimicrobiana nacional y monitoreo de programas,[59] monitoreo de las cantidades de antibióticos usados en la cría de animales,[60] y recomendaciones para asegurar la adecuada y prudente usan de sustancias antibióticas. Otra pauta introducido en el terrestre Código zoosanitario es la implementación de metodologías que ayuden a establecer los factores de riesgo asociados con esta preocupación en todo el mundo. La OIE concluyó que las evaluaciones de riesgo deben realizarse para evaluar, gestionar y definir los posibles riesgos de resistencia a los antibióticos en las poblaciones humanas y de animales.[61]
En el mundo, los antibióticos son ampliamente utilizados en los animales. Al igual que en medicina humana, los antibióticos a menudo pueden adquirirse sin receta médica y veterinaria supervisión para su uso en animales domésticos y ganado. Bacterias restantes en estos animales suelen ser resistentes a los antibióticos usados y pueden pasar al medio ambiente por la excreción y secreción de materiales tales como leche, heces, orina, saliva, semen, loquios, etc.. El impacto real de estos gérmenes resistentes depende de su tipo específico y en el animal o el organismo que en lo sucesivo infecten. Algunos gérmenes, como el tétanos, son tóxicos sin importar su estatus resistentes a los antibióticos. (Resulta útil recordar que los antibióticos no se utilizan en el tratamiento de todas las enfermedades causadas por bacterias. Tétanos, por ejemplo, se ve impedido por la vacuna y es extremadamente difícil de tratar una vez que aparezcan los síntomas).
En 1998, ministros de salud de la Unión Europea decidió prohibir cuatro antibióticos utilizados para promover el crecimiento animal (a pesar de las recomendaciones del grupo de los científicos[citación necesitada]). Reglamento prohíbe el uso de antibióticos en la alimentación Europea, con la excepción de dos antibióticos en la alimentación de las aves de corral, entró en vigor en 2006.[62] En Escandinavia, hay evidencia de que la prohibición ha llevado a una menor prevalencia de resistencia a los antimicrobianos en las poblaciones bacterianas animales (no peligrosos).[63] Sin embargo, un cambio correspondiente en los casos de resistencia a antibióticos entre los seres humanos todavía no ha sido demostrado.
Estados Unidos
En los Estados Unidos, la Departamento de agricultura de Estados Unidos (USDA) y la Food and Drug Administration (FDA) recogemos datos de uso de antibióticos en animales y seres humanos.[64] En estudios de investigación, ha demostrado ocasional animal al ser humano propagación de organismos resistentes a drogas. Los antibióticos y otros medicamentos se utilizan en piensos de Estados Unidos para promover la productividad animal.[12][65] En particular, agua y alimentación de las aves de corral es una ruta común de la administración de medicamentos, debido a mayores costos cuando se administran medicamentos por manipulación de los animales individualmente. En general, los animales que aparecen enfermos no se les permite ser sacrificados para el consumo humano en los Estados Unidos.
La creciente preocupación del consumidor estadounidense sobre el uso de antibióticos en la alimentación animal ha conducido a un nicho de mercado de productos de origen animal "sin antibióticos", pero este pequeño mercado es poco probable que cambien sus prácticas arraigadas, toda la industria.[66]
En 2001, la Union of Concerned Scientists estimó que más de 70% de los antibióticos utilizados en los Estados Unidos se dan a los animales alimentos (por ejemplo, pollos, cerdos y bovinos), en la ausencia de enfermedad.[67][22] Las cantidades dadas son llamadas "subterapéuticas", es decir, insuficiente para combatir la enfermedad. A pesar de no diagnóstico de la enfermedad, la administración de estos fármacos (la mayoría de los cuales no es significativa para la medicina humana) resulta en la disminución de la mortalidad y morbilidad y mayor crecimiento en los animales tratados así. La teoría es que las dosis subterapéuticas mata algunos, pero no todos, de los organismos bacterianos en el animal — probablemente dejando a aquellos que son naturalmente resistentes a los antibióticos[citación necesitada]. Estudios han demostrado, sin embargo, que, en esencia, los niveles de la población total de bacterias son invariables; Sólo la mezcla de bacterias se ve afectada.[citación necesitada]
Así está claro el mecanismo real por el cual servir subterapéuticas aditivos antibióticos como promotores del crecimiento. Algunas personas han especulado que los animales y las aves pueden tener infecciones subclínica, que se curaría por bajos niveles de antibióticos en los alimentos, permitiendo así que las criaturas prosperar. No se ha avanzado ninguna evidencia convincente para esta teoría, y la carga bacteriana en un animal es esencialmente sin cambios por el uso de antibióticos, aditivos para piensos. El mecanismo de promoción del crecimiento es por lo tanto probablemente algo más que "matar a los bichos malos."
En el año 2000, la FDA anunció su intención de revocar la aprobación de fluoroquinolona utilizar en la producción de aves de corral debido a evidencia sustancial vinculándolo a la aparición de fluoroquinolone-resistente Campylobacter infecciones en seres humanos. Legal retos del animal del alimento y las industrias farmacéuticas retrasa la decisión de hacerlo hasta el 2006.[68] Fluroquinolones han sido prohibidos de extra-etiquete el uso en la alimentación de animales en los Estados Unidos desde el año 2007. Sin embargo, siguen siendo ampliamente utilizados en la compañía y animales exóticos.
En 2001, National Hog Farmer revista advirtió a los productores estadounidenses que C. difficile "está arrasando en la industria, matando a muchos lechones" (Neutkens D; "Nuevo Clostridium alegando cerdos del bebé"). En 2006, un estudio National Animal salud sistema del USDA de monitoreo más investigó la prevalencia de C. difficile en granjas porcinas. El estudio, que cubre granjas porcícolas de tamaño típico de los que producen el 94% de los dos cerdos, halló la prevalencia de C. difficile "relativamente baja (11,4%)" y que no había ninguna diferencia en la región o en tamaño de granja.[69] Infección humana con C. difficile (ya sea resistente a los fármacos o no) es comúnmente asociado con el uso de antibióticos fuertes en los seres humanos hospitalizados y no está asociada con los seres humanos en contacto con animales de granja.
Durante el año 2007, dos proyectos de ley federales (S. 549[70] y H.R. 962[71]) destinadas a la eliminación gradual de los antibióticos "terapéuticos" en producción animal de alimentos de Estados Unidos. El proyecto de ley del Senado, presentado por el Sen. Edward "Ted" Kennedy, murió. Ley casa, presentado por Rep. Louise Slaughter, murió después de ser remitido a Comisión.
En los Estados Unidos, la FDA primero determinó en 1977 que hay evidencia de aparición de cepas bacterianas resistentes a los antibióticos en el ganado. La práctica largamente establecida de permitir las ventas de OTC de antibióticos (como la penicilina y otros medicamentos) a propietarios de animales para la administración de sus propios animales sin embargo continuó en todos los Estados. En marzo de 2012, el Tribunal de distrito de Estados Unidos para el distrito sur de Nueva York, gobernando en una acción judicial por la Natural Resources Defense Council y otros, ordenó a la FDA a revocar las aprobaciones para el uso de antibióticos en el ganado que violó las normas de la FDA.[72] El 11 de abril de 2012 la FDA anunció un programa voluntario para eliminar gradualmente el uso sin supervisión de drogas como aditivos para piensos y convertir usos aprobados sin receta para antibióticos recetados uso solamente, que requieren supervisión veterinaria de su uso y prescripción.[73][74] En diciembre de 2013, la FDA anunció el comienzo de estos pasos para eliminar gradualmente el uso de antibióticos para los fines de promover el crecimiento de la ganadería.[75][22]
Impacto ambiental
Los antibióticos han estado contaminando el medio ambiente desde su introducción a través de los desechos humanos (medicación, agricultura), los animales y la industria farmacéutica.[76] Junto con los residuos antibióticos, las bacterias resistentes a seguir, así introducir bacterias resistentes a los antibióticos en el medio ambiente. Como las bacterias replican rápidamente, las bacterias resistentes que entrar en el entorno replican sus genes de resistencia como siguen a dividir. Además, portadores de genes de resistencia de las bacterias tienen la capacidad para difundir esos genes de otras especies mediante transferencia horizontal del gene. Por lo tanto, incluso si el antibiótico específico ya no se introduce en el medio ambiente, los genes de resistencia a antibióticos persistirán a través de las bacterias que han replicado desde entonces sin la exposición continua.[76]
Un estudio de la Poudre River (Colorado, Estados Unidos) implicado en plantas de tratamiento de aguas residuales, así como las operaciones de alimentar los animales en la dispersión de genes de resistencia a antibióticos en el medio ambiente.[77] Esta investigación se realizó utilizando firmas moleculares para determinar las fuentes y la ubicación en el río de Poudre fue elegido debido a la falta de otras influencias antropogénicas aguas arriba. El estudio indica que control de genes de resistencia a antibióticos puede ser útil para determinar no sólo el punto de origen de su liberación, sino también cómo estos genes persisten en el medio ambiente. Además, estudiar métodos físicos y químicos del tratamiento puede aliviar la presión de los genes de resistencia a antibióticos en el medio ambiente y así su entrada en contacto humano.
Mecanismos

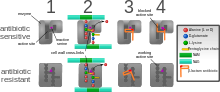
Resistencia a los antibióticos puede ser el resultado de transferencia horizontal de genes,[78] y también de disociados mutaciones puntuales en el patógeno genoma a un ritmo de aproximadamente 1 de cada 108 por replicación cromosómica. La acción antibiótica contra el patógeno puede verse como una presión ambiental. Esas bacterias con una mutación que les permite sobrevivir viven para reproducirse. Luego pasan esta característica a su descendencia, que conduce a la evolución de una colonia totalmente resistente.
Los cuatro principales mecanismos por los cuales microorganismos exhiben resistencia a los antimicrobianos son:
- Inactivación de drogas o modificación: por ejemplo, la desactivación enzimática de penicilina G en algunas bacterias resistentes a la penicilina a través de la producción de Β-lactamasas.
- Alteración del sitio de destino: por ejemplo, alteración de SB3— el sitio de destino obligatorio de penicilinas — en MRSA y otras bacterias resistentes a la penicilina
- Alteración de la vía metabólica: por ejemplo, algunos Sulfamida-no requieren de bacterias resistentes ácido para - aminobenzoico (PABA), un importante precursor de la síntesis de ácido fólico y ácidos nucleicos en bacterias inhibidas por las sulfamidas, en cambio, como las células mamíferas, convierten a usando el ácido fólico preformado.
- Reduce la acumulación de drogas: por la disminución de drogas permeabilidad o el aumento de activos emanación (bombear) de las drogas a través de la superficie celular[79]
Existen tres mecanismos conocidos de fluoroquinolona resistencia. Algunos tipos de emanación las bombas pueden actuar para disminuir intracelular quinolona concentración.[80] En las bacterias Gram-negativas, genes de resistencia mediada por plásmidos producen proteínas que pueden enlazar a ADN girasa, protegiéndolo de la acción de las quinolonas. Finalmente, las mutaciones en sitios claves de ADN girasa o Topoisomerasa IV puede disminuir su afinidad a las quinolonas, disminuyendo la eficacia de la droga.[81] La investigación ha demostrado que la proteína bacteriana LexA pueden desempeñar un papel clave en la adquisición de mutaciones bacterianas dando resistencia a quinolonas y rifampicina.[82]
Resistencia a los antibióticos también puede introducirse artificialmente en un microorganismo a través de los protocolos de laboratorio, utilizada a veces como un marcador seleccionable para examinar los mecanismos de transferencia de genes o para identificar a individuos que absorbe un trozo de ADN que incluía el gen de resistencia y otro gen de interés. Un estudio reciente demostró que el grado de transferencia horizontal de genes entre Estafilococo es mucho mayor de lo esperado previamente y abarca los genes con funciones más allá de la resistencia a los antibióticos y virulencia y más allá de los genes que reside dentro de la elementos genéticos móviles.[83]
Durante mucho tiempo, se ha pensado que, para que un microorganismo que se vuelven resistentes a un antibiótico, debe ser en una población grande. Sin embargo, descubrimientos recientes demuestran que no hay ninguna necesidad de grandes poblaciones de bacterias para la aparición de resistencia a los antibióticos. Ahora sabemos que pequeñas poblaciones de e. coli en un gradiente de antibiótico pueden volverse resistentes. Cualquier entorno heterogéneo con respecto a los gradientes de nutrientes y antibióticos puede facilitar el desarrollo de resistencia a antibióticos en poblaciones bacterianas pequeñas y esto también es válido para el cuerpo humano. Los investigadores presumen que el mecanismo de desarrollo de la resistencia se basa en cuatro mutaciones de SNP en el genoma de e. coli producida por el gradiente del antibiótico. Estas mutaciones confieren la aparición de bacterias de resistencia a los antibióticos.
Una idea falsa común es que una persona puede volverse resistente a ciertos antibióticos. Es una cepa de microorganismo que puede volverse resistente, no el cuerpo de una persona.[84][85]
Patógenos resistentes
Estafilococo áureo
Estafilococo áureo (coloquialmente conocido como "Staphylococcus aureus" o una "infección") es uno de los principales agentes patógenos. Encontrado en el membranas mucosas y el piel humana de alrededor de un tercio de la población, es muy adaptable a presión antibiótica. Fue una de las bacterias antes de que penicilina se encontró resistencia — en 1947, apenas cuatro años después de la droga comenzó a ser producido en masa. Meticilina luego fue el antibiótico de elección, pero desde entonces ha sido reemplazado por oxacilina debido a la toxicidad renal significativa. Resistente a la meticilina Estafilococo áureo (MRSA) se detectó primero en Gran Bretaña en 1961 y ahora es "muy común" en los hospitales. MRSA era responsable del 37% de casos fatales de sepsis En UK en 1999, frente al 4% en 1991. La mitad de todos S. aureus las infecciones en las US son resistentes a la penicilina, meticilina, tetraciclina y eritromicina.
Esta izquierda vancomicina como el agente sólo eficaz disponible en el momento. Sin embargo, las cepas con niveles intermedio (4-8 µg/ml) de resistencia, denominada glicopéptido-intermedio Estafilococo áureo (GISA) o vancomicina-intermedio Estafilococo áureo (VISA), comenzó a aparecer en la década de 1990. El primer caso identificado fue en Japón en 1996, y desde entonces han encontrado cepas en hospitales de Inglaterra, Francia y Estados Unidos. El primero documentado cepa con completa (> 16 µg/ml) resistencia a la vancomicina, denominado resistente a la vancomicina Estafilococo áureo (VRSA) apareció en los Estados Unidos en 2002.[86] Sin embargo, en 2011, una variante de la vancomicina ha sido probada que se une a la variación de lactato y también se une así a la meta original, reinstaurando así potente actividad antimicrobiana.[87]
Una nueva clase de antibióticos, oxazolidinonas, llegó a estar disponible en los años 90 y el primer oxazolidinonas comercialmente disponibles, linezolid, es comparable a la vancomicina en efectividad contra MRSA. Resistencia a linezolid en S. aureus se reportó en 2001.[88]
MRSA extrahospitalaria (CA-MRSA) ahora se ha convertido en una epidemia que es responsable de enfermedades rápidamente progresivas, fatales, incluyendo neumonía severa necrotizante sepsis, y fascitis necrotizante.[89] MRSA es el patógeno resistente a los medicamentos antimicrobiano más frecuentemente identificado en los hospitales de Estados Unidos. El Epidemiología de las infecciones causadas por MRSA está cambiando rápidamente. En los últimos 10 años[¿Cuándo?], las infecciones causadas por este organismo han surgido en la comunidad. Los dos clones MRSA en los Estados Unidos más estrechamente asociados a brotes de comunidad, USA400 (Cepa MW2, linaje ST1) y USA300, a menudo contienen Panton-Valentine leukocidin Los genes (PVL) y, más frecuentemente, se han asociado con la piel e infecciones de tejidos blandos. Brotes de infecciones de CA-MRSA se han divulgado en centros penitenciarios, entre los equipos atléticos, los reclutas militares, en salas de recién nacidos y entre los hombres que tienen sexo con hombres. CA-MRSA infecciones ahora aparecen endémicas en muchas regiones urbanas y provocar más CA-S. aureus infecciones.[90]
Estreptococo y Enterococo
Streptococcus pyogenes (Grupo A Estreptococo:: GAS) infecciones generalmente pueden ser tratadas con muchos antibióticos diferentes. El tratamiento temprano puede reducir el riesgo de muerte por una enfermedad por estreptococo grupo invasor. Sin embargo, incluso los mejores cuidados médicos no impide la muerte en cada caso. Para aquellos con enfermedades muy graves, se pueden necesitar cuidados médicos de apoyo en una unidad de cuidados intensivos. Para las personas con fascitis necrotizante, a menudo se requiere cirugía para extirpar el tejido dañado.[91] Cepas de S. pyogenes resistente a la macrólidos los antibióticos han surgido; Sin embargo, permanecen uniformemente susceptibles a todas las cepas penicilina.[92]
Resistencia de Estreptococo pneumoniae a la penicilina y otros beta-lactámicos está aumentando en todo el mundo. El principal mecanismo de resistencia consiste en la introducción de mutaciones en genes que codifican para proteínas de unión a penicilina. Presión selectiva se piensa para desempeñar un papel importante, y uso de antibióticos beta-lactámicos se ha implicado como un factor de riesgo para la infección y colonización. S. pneumoniae es responsable de neumonía, bacteriemia, otitis media, meningitis, sinusitis, peritonitis y artritis.[92]
Multirresistente Enterococo faecalis y Enterococcus faecium están asociados con infecciones nosocomiales.[93] Entre estas cepas, penicilina-resistente Enterococo fue visto en 1983, resistente a la vancomicina Enterococo en 1987, y linezolid-resistente Enterococo en la década de 1990.[citación necesitada]
Pseudomonas aeruginosa
Pseudomonas aeruginosa es un altamente prevalente patógeno oportunista. Una de las características más preocupantes de P. aeruginosa es su baja sensibilidad a los antibióticos, que se puede atribuir a una acción concertada de bombas de eflujo multirresistente con cromosómico codificada en los genes de resistencia a los antibióticos (por ejemplo, mexAB-oprM, mexXYetc..) y la baja permeabilidad de los sobres celulares bacterianas.[94] Pseudomonas aeruginosa tiene la capacidad de producir 4-hidroxi-2-alkylquinolines (HAQs) y se ha encontrado que HAQs tienen efectos prooxidantes y overexpressing modestamente mayor susceptibilidad a los antibióticos. El estudio experimentó con la Pseudomonas aeruginosa los biofilms y encontró que una interrupción de genes relA y punto produce una inactivación de la respuesta estricta (SR) en células con limitación de nutrientes, que proporciona las células son más susceptibles a los antibióticos.[95]
El Clostridium difficile
El Clostridium difficile es un patógeno nosocomial que provoca la enfermedad diarreica en todo el mundo los hospitales.[96][97]
C. difficile la colitis es más fuertemente asociada con fluoroquinolonas, cefalosporinas, carbapenemes, y clindamicina.[98][99][100] El Centro Europeo para el Control y prevención de enfermedades recomendamos las fluoroquinolonas y el antibiótico clindamicina evitarse en la práctica clínica debido a su alta asociación con CDI.[citación necesitada]
Algunas investigaciones sugieren que el uso excesivo de antibióticos en la cría de ganado está contribuyendo a los brotes de infecciones bacterianas como C. difficile.[16]
Antibióticos, especialmente aquellas con un espectro amplio de actividad (por ejemplo, clindamicina) alteran la flora intestinal normal. Esto puede conducir a una proliferación de C. difficile, que florece en estas condiciones. Colitis seudomembranosa puede seguir creando inflamación generalizada del colon y el desarrollo de "pseudomembrana", una colección viscosa de fibrina, células inflamatorias y células necróticas.[4] Clindamicina-resistente C. difficile se informó que el agente causal de grandes brotes de enfermedades diarreicas en los hospitales de Nueva York, Arizona, Florida y Massachusetts entre 1989 y 1992.[101] Brotes dispersos geográficamente de C. difficile cepas resistentes a fluoroquinolona antibióticos como la ciprofloxacina y la levofloxacina, también se reportaron en América del norte en 2005.[102]
Salmonella y E. coli
Infección con Escherichia coli y Salmonella puede provocar el consumo de agua y alimentos contaminados. Cuando ambas bacterias se extienden, se presentan condiciones graves de salud. Muchas personas son hospitalizadas cada año después de infectarse, con algunos mueren como resultado. Desde 1993, algunas cepas de E. coli se han vuelto resistentes a múltiples tipos de antibióticos de fluoroquinolona.[citación necesitada]
Acinetobacter baumannii
El 05 de noviembre de 2004, la Centers for Disease Control and Prevention (CDC) informó de un número creciente de Acinetobacter baumannii infecciones del torrente sanguíneo en pacientes en las instalaciones médicas militares en el que los miembros del servicio heridos en la Irak/Kuwait región durante Operación Libertad iraquí y en Afganistán durante Operación libertad duradera fueron tratados. Mayoría de estos mostraron multirresistencia (MRAB), con algunos aislamientos resistentes a todos los fármacos probados.[103][104]
Klebsiella pneumoniae
Klebsiella pneumoniae carbapenemase)KPC)-bacterias productoras son un grupo de emergentes bacilos gramnegativos altamente resistente a los medicamentos que causan infecciones asociadas con importante morbilidad y mortalidad, cuya incidencia está aumentando rápidamente en una variedad de ajustes clínicos alrededor del mundo. Klebsiella pneumoniae incluye numerosos mecanismos de resistencia a los antibióticos, muchos de los cuales se encuentran en los elementos genéticos móviles altamente.[105] Carbapenems antibióticos (hasta ahora a menudo el tratamiento de último recurso para las infecciones resistentes) generalmente no son efectivos contra organismos productores de KPC.[106]
Tuberculosis del Mycobacterium
Tuberculosis está aumentando en todo el mundo, especialmente en los países en desarrollo, en los últimos años. Se llama TB resistente a los antibióticos TUBERCULOSIS MDR (TB multirresistentes). A nivel mundial, MDR TB causa 150.000 muertes anualmente.[107] El surgimiento de la epidemia del VIH/SIDA ha contribuido a esto.[108]
TB fue considerada una de las enfermedades más prevalentes y no tenía hasta el descubrimiento de una cura Estreptomicina por Selman Waksman en 1943.[109] Sin embargo, las bacterias pronto desarrollaron resistencia. Desde entonces, las drogas tales como isoniazida y rifampicina se han utilizado. M. tuberculosis desarrolla resistencia a los medicamentos por mutaciones espontáneas en sus genomas. Resistencia a un medicamento es común, y por esta razón el tratamiento se realiza generalmente con más de una droga. Tuberculosis extremadamente farmacorresistente (XDR TB) es TB que es resistente a la segunda línea de medicamentos.[108][110]
Resistencia de Tuberculosis del Mycobacterium Para isoniazida, rifampicina, y otros tratamientos comunes se ha convertido en un desafío clínico cada vez más relevante. (Para más información sobre la tuberculosis farmacorresistente, visite el Tuberculosis resistente a múltiples fármacos página.)
Neisseria gonorrhoeae
| Esta sección requiere expansión con: información del artículo principal. (Noviembre de 2013) |
Neisseria gonorrhoeae es un patógeno de transmisión sexual que puede causar dolor pélvico, dolor al orinar, del pene y descarga vaginal, así como síntomas sistémicos en la infección humana. La bacteria se identificó primero en 1879,[111] Aunque algunos estudiosos bíblicos creen que se pueden encontrar referencias a la enfermedad tan pronto como Parshat Metzora de la Antiguo Testamento.[112]
Tratamiento con penicilina en la década de 1940 demostró ser útil, pero por las cepas resistentes de los años setenta predominaron. Resistencia a la penicilina se ha desarrollado a través de dos mecanismos: chomasomally mediada por resistencia (CMRNG) y la resistencia mediada por penicilinasa (Penicilinasa). CMRNG implica mutación progresivo de la penA, que codifica para la proteína de unión a penicilina (PBP-2); MTR, que codifica una bomba de eflujo para quitar la penicilina de la célula; y penB, que codifica las Porinas de la pared celular bacteriana. Penicilinasa implica la adquisición de un plásmido transmitidas por beta-lactamasa.[113] Fluoroquinolonas eran un tratamiento útil siguiente línea hasta que la resistencia se logró a través de bombas de eflujo y mutaciones en el gen gyrA, que codifica ADN girasa.[113] Cefalosporinas de tercera generación han utilizado para tratar la gonorrea desde 2007, aunque han surgido cepas resistentes. También se han encontrado cepas de Neisseria gonorrea resistentes al tetraciclinas y aminoglucósidos. Neisseria gonorrheoea tiene una alta afinidad para la transferencia horizontal de genes, y como resultado, la existencia de cualquier cepa resistente a un fármaco determinado podría extenderse fácilmente a través de las cepas. Hoy en día, ceftriaxona inyectable se utiliza, a veces en combinación con azitromicina o doxiciclina.[114][115]
Prevención
Recomendaciones de la organización de salud mundial
Un informe del 30 de abril de 2014, por la QUE hace las siguientes recomendaciones sobre cómo abordar la resistencia a los antibióticos:[2]
- La gente puede ayudar frente resistencia por:
- uso de antibióticos solamente cuando lo prescribe un médico;
- completando la receta completa, incluso si se sienten mejor;
- Nunca compartir los antibióticos con los demás o usando recetas sobrantes.
- Farmacéuticos y trabajadores de la salud pueden ayudar a abordar la resistencia por:
- mejorar la prevención de infecciones y control;
- prescripción y dispensación de antibióticos cuando verdaderamente son necesarios;
- prescripción y dispensación la derecha antibióticos para tratar la enfermedad.
- Las autoridades pueden ayudar a abordar la resistencia por:
- fortalecer el seguimiento de la resistencia y la capacidad de laboratorio;
- regular y promover el adecuado usan de los medicamentos.
- Las autoridades y la industria pueden ayudar a abordar la resistencia por:
- fomentar la innovación, investigación y desarrollo de nuevas herramientas;
- promover la cooperación y el intercambio de información entre todas las partes interesadas.
Prevención de infecciones
Uso racional de antibióticos puede reducir las posibilidades de desarrollo de infecciones oportunistas por bacterias resistentes a los antibióticos debido a disbacteriosis. Nuestro sistema inmunológico curará infecciones bacterianas leves por su propia cuenta. Si nos dan la oportunidad sin depender de los antibióticos para curar una pequeña infección, será menos probable que se vuelven inmunes o resistentes a los antibióticos. También es importante señalar que los antibióticos no curará infecciones virales como la gripe y los resfriados, y tomando un antibiótico innecesariamente para tratar una infección viral puede conducir a la resistencia de los antibióticos[116] En un estudio, está claramente asociado con el uso de fluoroquinolonas El Clostridium difficile infección, que es una de las principales causa de nosocomial diarrea en los Estados Unidos,[117] y una causa importante de muerte en todo el mundo.[118]
Vacunas No tienen el problema de la resistencia porque una vacuna refuerza las defensas naturales del cuerpo, mientras que un antibiótico funciona por separado de las defensas del cuerpo normal. Sin embargo, nuevas cepas que escapar la inmunidad inducida por las vacunas pueden evolucionar; por ejemplo, una versión actualizada vacuna contra la influenza se necesita cada año.
Mientras que teóricamente prometedor, antiestafilocócicas vacunas han demostrado eficacia limitada, debido a la variación inmunológica entre Estafilococo especies y la duración limitada de la eficacia de los anticuerpos producidos. Desarrollo y pruebas de vacunas más efectivas está en marcha.[119]
La investigación científica e Industrial de Commonwealth australiana (organizaciónCSIRO), consciente de la necesidad para la reducción del uso de antibióticos, ha estado trabajando en dos alternativas. Una alternativa es para prevenir las enfermedades mediante la adición de citoquinas en lugar de antibióticos para la alimentación animal.[120] Estas proteínas se realizan en el cuerpo animal "naturalmente" después de una enfermedad y no son los antibióticos, lo que no contribuyen al problema de la resistencia a los antibióticos. Además, los estudios sobre el uso de las citoquinas han mostrado también mejorar el crecimiento de animales como los antibióticos usados ahora, pero sin las desventajas del uso de antibióticos terapéuticos. Las citoquinas tienen el potencial para alcanzar las tasas de crecimiento animal buscadas tradicionalmente por el uso de antibióticos sin la contribución de la resistencia antibiótica asociada a los usos terapéuticos generalizados de los antibióticos utilizados actualmente en las industrias de producción animal de alimentos. Además, CSIRO está trabajando en vacunas contra las enfermedades.[120]
Terapia phage
Terapia phage, un enfoque que ha sido ampliamente investigado y utilizado como un agente terapéutico para más de 60 años, especialmente en el Unión Soviética, representa un enfoque actualmente subdesarrollado pero potencialmente significativo para el tratamiento de las enfermedades bacterianas.[121] Terapia phage fue utilizada ampliamente en los Estados Unidos hasta el descubrimiento de los antibióticos, en los años 40 tempranos. Los bacteriófagos o "fagos" son virus que invaden las células bacterianas y, en el caso de fagos líticas, perturban el metabolismo bacteriano y causan la bacteria Lyse. La terapia phage es el uso terapéutico de lítica bacteriófagos para el tratamiento de patógenos infecciones bacterianas.[122] [123] [124]
Bacteriófago terapia es una alternativa a los antibióticos potencialmente importante en la época actual de patógenos multirresistentes. Una revisión de estudios que abordan el uso terapéutico de fagos de 1966 a 1996 y algunos proyectos de terapia de último curso fago vía internet mostró: fagos fueron utilizados por vía tópica, oral o sistémica en estudios polacos y soviéticos. La tasa de éxito en estos estudios fue 80 – 95%, con pocos efectos secundarios gastrointestinales o alérgicos. Los estudios británicos también demostraron una eficacia significativa de fagos contra Escherichia coli, Acinetobacter spp., Pseudomonas spp., y Estafilococo áureo. Estudios de Estados Unidos tratados de mejorar la biodisponibilidad de fagos. Terapia phage puede resultar como una importante alternativa a los antibióticos para el tratamiento de patógenos multirresistentes.[125]
Descubrimiento de la estructura de la proteína viral PlyC está permitiendo a los investigadores a entender cómo mata una significativa variedad de bacterias patógenas.[126]
Investigación
Desarrollo
Desde el descubrimiento de los antibióticos, investigación y desarrollo Esfuerzos (R & D) han proporcionado nuevos medicamentos en el tiempo para tratar las bacterias que se convirtieron en resistentes a los antibióticos más viejos, pero en la década pasada ha habido preocupación por desarrollo ha disminuido bastante que gravemente enfermos pueden ejecutar fuera de las opciones de tratamiento.[127] Otra preocupación es que los médicos pueden llegar a ser reacios a realizar cirugías de rutina debido al riesgo aumentado de infección dañina.[128] Tratamientos de copia de seguridad pueden tener efectos secundarios graves; por ejemplo, tratamiento de la tuberculosis resistente a múltiples fármacos puede causar sordera y demencia.[129] La potencial crisis de mano es el resultado de una disminución marcada en la industria R & D.[130] Pobre inversión financiera en investigación de antibiótico ha agravado la situación.[130][22] En 2011, Pfizeruno de las últimas grandes compañías farmacéuticas desarrollar nuevos antibióticos, cerró su esfuerzo de investigación primaria, citando accionista pobre devuelve relativa a medicamentos para enfermedades crónicas.[131]
En los Estados Unidos, las compañías farmacéuticas y la administración de Presidente Barack Obama han venido planteando cambiar las normas por las cuales la FDA aprueba dirigidos a organismos resistentes a los antibióticos.[128][132] El 12 de diciembre de 2013, el desarrollo de antibióticos a avanzar paciente tratamiento (ADAPT) acto de 2013 se introdujo en el Congreso de Estados Unidos. La ley ADAPT pretende acelerar el desarrollo de medicamentos para combatir la creciente amenaza de salud pública de 'superbacterias'. Bajo esta ley, la FDA puede aprobar los antibióticos y antifúngicos para infecciones potencialmente mortales en base a datos de los ensayos clínicos más pequeños. El CDC reforzará la vigilancia del uso de antibióticos que tratan graves infecciones peligrosas para la vida y la resistencia emergente y hacer que los datos disponibles al público. Los antibióticos FDA etiquetado proceso, 'Susceptibilidad prueba criterios interpretativos para organismos microbianos' o 'ruptura' también se optimiza para permitir la más actualizados y de vanguardistas datos disponibles para profesionales de la salud bajo la nueva ley.[133][134]
Los Estados Unidos Institutos nacionales de salud planes para financiar una nueva red de investigación sobre el tema hasta $ 62 millones de 2013 al 2019.[135] Uso de la autoridad creada por la Pandemia y todo acto de preparación para los peligros de 2006, la Investigación biomédica avanzada y Desenvolvemento en los Estados Unidos Departamento de salud y servicios humanos anunció que gastará entre $ 40 millones y $ 200 millones en fondos para i+d de nuevos antibióticos en desarrollo por GlaxoSmithKline.[136]
Mecanismo
En la investigación publicada el 17 de octubre de 2008 en Celular, un equipo de científicos identificó el lugar de las bacterias donde el antibiótico myxopyronin lanza su ataque, y por ese ataque es exitoso. El myxopyronin se une a e inhibe la enzima bacteriana crucial ARN polimerasa. El myxopyronin cambia la estructura del segmento conmutador-2 de la enzima, inhibiendo su función de lectura y transmitir el código de ADN. Esto evita que la ARN polimerasa entregando información genética para el ribosomas, que causan las bacterias a morir.[137]
En 2012, un equipo de la Universidad de Leipzig modificado un péptido que se encuentra en las abejas. Es eficaz contra 37 tipos de bacterias.[138]
Una causa importante de resistencia a los antibióticos es la mayor actividad de bombeo de microbiana Transportadores ABC, que disminuye la concentración de fármaco eficaz dentro de la célula microbiana. Inhibidores de transportador ABC que pueden utilizarse en combinación con antimicrobianos actuales se están probando en ensayos clínicos y están disponibles para los regímenes terapéuticos.[139]
Aplicaciones
Resistencia a los antibióticos es una herramienta importante para ingeniería genética. Mediante la construcción de un plásmido que contiene un gen de resistencia a antibióticos, como el gen diseñado o expresado, un investigador puede asegurar que, cuando las bacterias replican, sólo los ejemplares que llevan el plásmido sobreviven. Esto garantiza que el gen había manipulado pasos cuando reproduce las bacterias.
En general, los antibióticos más utilizados en la ingeniería genética son antibióticos "mayores" que han caído en gran medida fuera de uso en la práctica clínica. Estos incluyen:
- ampicilina
- kanamicina
- tetraciclina
- cloranfenicol
En la industria, el uso de la resistencia a los antibióticos es desfavorecido, desde mantenimiento de cultivos bacterianos requeriría dándoles de comer grandes cantidades de antibióticos. En cambio, el uso de auxotrophic función-reemplazo plásmidos (y cepas bacterianas) es preferido.
Véase también
- Alianza para el uso prudente de antibióticos
- Jabón antibacteriano
- #KPC (K. pneumoniae carbapenemase) beta-lactamasa (clase A) Gen de resistencia antibacteriana (KPC)
- Antibiótico de amplio espectro
- Enterobacterias resistentes a carbapenem
- Centro para la dinámica de la enfermedad, economía y política
- Drogas de último recurso
- Índice de artículos del medio ambiente
- La tolerancia
- Bacterias Gram-negativas multirresistentes
- Nueva Delhi metalo-beta-lactamasa Gen de resistencia antibacteriana (NDM-1)
- Resistencia a pesticidas
Notas al pie
- ^ "Resistencia a los antibióticos preguntas & respuestas". Get Smart: Saber cuando los antibióticos. Centers for Disease Control and Prevention, Estados Unidos. 30 de junio de 2009. 20 de marzo de 2013.
- ^ a b "¿Quién es el primer informe mundial sobre la resistencia a los antibióticos revela en todo el mundo, seria amenaza para la salud pública" Obtenido 2014-05-02
- ^ a b Zainuddin ZF, Dale JW (1990). "Mycobacterium tuberculosis tiene plásmidos?". Tubérculo 71 (1): 43 – 9. Doi:10.1016/0041-3879 (90) 90060-l. PMID2115217.
- ^ GE Louw, Warren RM, Gey van Pittius NC, CR McEvoy, Van Helden PD, Victor TC (2009). "Un ejercicio de malabarismo: emanación/afluencia en resistencia a los medicamentos por micobacterias". Agentes antimicrobianos y quimioterapia 53 (8): 3181 – 9. Doi:10.1128/AAC.01577-08. PMC2715638. PMID19451293.
- ^ D'Costa et al., 2011, págs. 457-461.
- ^ Donadio et al., 2010, págs. 423-430.
- ^ Caldwell & Lindberg 2011.
- ^ Nelson 2009, p. 294.
- ^ Hawkey & Jones 2009, págs. i3-i10.
- ^ Goossens H, Ferech M, Vander Stichele R, Elseviers M (2005). "El uso de antibióticos para pacientes ambulatorios en Europa y en asociación con resistencia: un estudio de base de datos transnacionales". The Lancet 365 (9459): 579 – 87. Doi:10.1016/S0140-6736 (05) 17907-0. PMID15708101.
- ^ Ferber D (04 de enero de 2002). "Ganadería alimente Ban conservas de medicamentos". Ciencia 295 (5552): 27 – 28. Doi:10.1126/science.295.5552.27A. PMID11778017.
- ^ a b Mathew AG, Cissell R, Liamthong S; Cissell, R; Liamthong, S (2007). "Resistencia a los antibióticos en las bacterias asociadas con los animales de alimentos: una perspectiva de Estados Unidos de la producción ganadera". Pathog transmitidas por los alimentos. Dis. 4 (2): 115 – 33. Doi:10.1089/FpD.2006.0066. PMID17600481.
- ^ CDC. ¿"Antibióticos resistencia preguntas & respuestas" [son antibacterianos que contienen productos (jabones, limpiadores, etc.) mejor para prevenir la propagación de la infección? Su uso Aporta al problema de la resistencia?]. Atlanta, Georgia, USA.: Centers for Disease Control and Prevention. Programa archivado de la original en 08 de noviembre de 2009. 17 de noviembre de 2009.
- ^ Larsson DG, Fick J (enero de 2009). "La transparencia a lo largo de la cadena de producción, una forma de reducir la contaminación de la fabricación de productos farmacéuticos?". Regul Toxicol Pharmacol 53 (3): 161-3. Doi:10.1016/j.yrtph.2009.01.008. PMID19545507.
- ^ Infecciones relacionadas con la salud
- ^ "Resistencia a los antibióticos". Sciencedaily.com. 2013-06-12.
- ^ Tacconelli E, De Angelis G, MA Cataldo, Pozzi E, Cauda R (enero de 2008). "¿Antibiótica exposición aumentan el riesgo de resistente a la meticilina aislamiento de Staphylococcus aureus (MRSA). Una revisión sistemática y meta-análisis". J Antimicrob. Chemother. 61 (1): 26 – 38. Doi:10.1093/jac/dkm416. PMID17986491.
- ^ SER Muto CA, Jernigan JA, Ostrowsky, Richet HM, Jarvis WR, Boyce JM, Farr BM (mayo de 2003). "Pauta SHEA para la prevención de la transmisión nosocomial de cepas multirresistentes de Staphylococcus aureus y enterococcus". Control Hosp Epidemiol infectar 24 (5): 362 – 86. Doi:10.1086/502213. PMID12785411.
- ^ Vonberg, Dr. Ralf-Peter. "Clostridium difficile: un desafío para los hospitales". Centro Europeo para el Control y prevención de enfermedades. Instituto de Microbiología médica y epidemiología hospitalaria: IHE. Programa archivado de la original en 11 de junio de 2009. 27 de julio de 2009.
- ^ EJ Kuijper, van Dissel JT, Wilcox MH; van Dissel, J.; Wilcox, MH (agosto de 2007). "Clostridium difficile: cambio de Epidemiología y nuevas opciones de tratamiento". Opinión actual de las enfermedades infecciosas 20 (4): 376-83. Doi:10.1097/QCO.0b013e32818be71d. PMID17609596.
- ^ editores, Ronald Eccles, Olaf Weber, (2009). Resfriado común (Online-Ausg. ed.). Basilea: Birkhäuser. p. 240. ISBN978-3-7643-9894-1.
- ^ a b c d Martin Khor (2014-05-18). "¿Por qué son los antibióticos cada vez inútiles en todo el mundo?". Las noticias reales. 2014-05-18.
- ^ a b c Wright GD (octubre de 2010). "Resistencia a los antibióticos en el medio ambiente: un enlace a la clínica?". Current Opinion in Microbiology 13 (5): 589 – 94. Doi:10.1016/j.MIB.2010.08.005. PMID20850375.
- ^ "Las mutaciones son al azar". Universidad de California. 14 de agosto de 2011.
- ^ Richard William Nelson. Darwin, entonces y ahora: la historia más increíble de la historia de la ciencia, iUniverse, 2009, p. 294
- ^ Wayne W. Umbreit, Avances en la Microbiología Aplicada, vol. 11, Academic Press, 1970, p. 80
- ^ Sr. Pollock (1967). "Origen y función de penicilinasa: un problema en la evolución bioquímica". British Medical Journal 4 (5571): 71-7. Doi:10.1136/bmj.4.5571.71. PMC1748446. PMID4963324.
- ^ a b New Scientist8 de Jun de 1972, p. 546
- ^ a b New Scientist11 de Feb de 1989, p. 34
- ^ Pollock, p. 77
- ^ Abigail A. Salyers, D. Dixie Whitt. La venganza de los microbios: Cómo la resistencia bacteriana está socavando el milagro antibióticoASM Press, 2005, p. 34
- ^ Pechère JC (septiembre de 2001). "Los pacientes entrevistas y uso indebido de los antibióticos". Clin. Infectar. Dis. 33 Suppl 3: S170 – 3. Doi:10.1086/321844. PMID11524715.
- ^ Arnold SR, Straus SE; Straus, SE (2005). "Las intervenciones para mejorar las prácticas de prescripción antibióticas en atención ambulatoria". En Arnold, Sandra R. Cochrane Database of Systematic Reviews (4): CD003539. Doi:10.1002/14651858.CD003539.pub2. PMID16235325.
- ^ McNulty CA, Boyle P, Nichols T, Clappison P, Davey P (agosto de 2007). El público actitudes y cumplimiento con antibióticos. J Antimicrob. Chemother. 60 supl 1: i63 – 8. Doi:10.1093/jac/dkm161. PMID17656386.
- ^ editores, Ronald Eccles, Olaf Weber, (2009). Resfriado común (Online-Ausg. ed.). Basilea: Birkhäuser. p. 234. ISBN978-3-7643-9894-1.
- ^ C Costelloe, Metcalfe C, A, D, Mant, Lovering heno AD (2010). "Efecto de la prescripción de antibióticos en atención primaria en resistencia a los antimicrobianos en pacientes individuales: revisión sistemática y meta-análisis". British Medical Journal 340:: c2096. Doi:10.1136/bmj.c2096. PMID20483949.
- ^ Li JZ, Winston LG, Moore DH, doblado S (septiembre de 2007). "Eficacia de corta duración regímenes de antibióticos para la neumonía adquirida en la comunidad: un meta-análisis". Soy J. Med. 120 (9): 783 – 90. Doi:10.1016/j.amjmed.2007.04.023. PMID17765048.
- ^ BIGNARDI GE (31 de agosto de 1998). "Factores de riesgo para la infección por Clostridium difficile". Journal of Hospital Infection 40 (1): 1 – 15. Doi:10.1016/S0195-6701 (98) 90019-6. PMID9777516.
- ^ Runyon BA McHutchison JG, Antillón MR, Akriviadis EA, Montano AA (junio de 1991). "Corta duración versus el tratamiento antibiótico de larga duración de peritonitis bacteriana espontánea. Un estudio controlado aleatorio de 100 pacientes". Gastroenterología 100 (6): 1737 – 42. PMID2019378.
- ^ N Singh, Rogers P, Atwood CW, Wagener MM, Yu VL (01 de agosto de 2000). "El tratamiento antibiótico empírico de corta duración para los pacientes con pulmonar infiltrados en la unidad de cuidados intensivos una solución propuesta para la prescripción de antibiótico indiscriminado". AM j Respir. Crit. Care Med. 162 (2): 505-511. Doi:10.1164/ajrccm.162.2.9909095. PMID10934078.
- ^ AL Gleisner, Argenta R, Pimentel M, Simon TK, Jungblut CF, Petteffi L, RM de Souza, Sauerssig M, CD Kruel, Machado AR (30 de abril de 2004). "Las complicaciones infecciosas según la duración del tratamiento antibiótico en el abdomen agudo". Revista Internacional de enfermedades infecciosas 8 (3): 155-162. Doi:10.1016/j.ijid.2003.06.003. PMID15109590.
- ^ Pichichero ME, Cohen R (1997). "Acortado curso de terapia con antibióticos para la otitis media aguda, sinusitis y tonsillopharyngitis". La revista de enfermedades infecciosas pediátricas 16 (7): 680 – 95. Doi:10.1097/00006454-199707000-00011. PMID9239773.
- ^ Dellinger EP, Wertz MJ, Lennard ES, señor Oreskovich (1986). "La eficacia de la profilaxis antibiótica de corta duración después de lesión Intestinal penetrante". Archivos de cirugía 121 (1): 23 – 30. Doi:10.1001/archsurg.1986.01400010029002. PMID3942496.
- ^ B Perez-Gorricho, Ripoll M (2003). "Terapia antibiótico de corta duración mejor cumple las expectativas del paciente?". Revista Internacional de agentes antimicrobianos 21 (3): 222 – 8. Doi:10.1016/S0924-8579 (02) 00360-6. PMID12636982.
- ^ Keren R, Chan E (2002). "Un metanálisis de ensayos controlados aleatorios que compararon el tratamiento antibiótico corta y larga duración para infecciones del tracto urinario en los niños". Pediatría 109 (5): E70 – 0. Doi:10.1542/peds.109.5.E70. PMID11986476.
- ^ McCormack J, Allan GM (2012). "Una receta para mejorar la prescripción de antibióticos en atención primaria". British Medical Journal 344:: d7955. Doi:10.1136/bmj.d7955. PMID22302779.
- ^ Marc Bonten, MD; Eijkman-Winkler Instituto para microbiología médica, enfermedades infecciosas y la inflamación; Utrecht, los Países Bajos | https://hicsigwiki.ASID.net.au/images/4/41/Should_you_stop_an_antibiotic_course_early_if_you_feel_better_R._Everts.pdf
- ^ Thomas JK A Forrest, Bhavnani SM, Hyatt JM, Cheng A, Ballow CH, Schentag JJ (marzo de 1998). "Evaluación farmacodinámica de factores asociados con el desarrollo de resistencias bacterianas en pacientes gravemente enfermos durante la terapia". Antimicrob. Agentes Chemother. 42 (3): 521 – 7. PMC105492. PMID9517926.
- ^ Girou E, Legrand P, hacienso-Altrach S, Lemire A, C Poulain, Allaire A, Tkoub-Scheirlinck L, Chai SH, C Dupeyron, Loche CM (octubre de 2006). "La asociación entre el cumplimiento de la higiene de manos y resistente a la meticilina Staphylococcus aureus prevalencia en un hospital de rehabilitación francés". Control Hosp Epidemiol infectar 27 (10): 1128 – 30. Doi:10.1086/507967. PMID17006822.
- ^ Swoboda SM, Earsing K, Strauss K, Lane S, PA Lipsett (febrero de 2004). Avisos voz y monitoreo electrónicos mejoran la higiene de las manos y disminución de las infecciones nosocomiales en una unidad de cuidados intermedios. Crit. Care Med. 32 (2): 358 – 63. Doi:10.1097/01.CCM.0000108866.48795.0F. PMID14758148.
- ^ Farmer, Paul E., Bruce Nizeye, Sara Stulac y Salman Keshavjee. 2006. violencia estructural y la medicina clínica. PLoS Medicine, 1686 – 1691.
- ^ El fenómeno de la resistencia de los microbios y vectores de enfermedades infecciosas: implicaciones para la salud humana y las estrategias para la contención: Resumen del taller. Instituto de medicina (Estados Unidos) Foro sobre infecciones emergentes; Najafi Knobler SL, SM limón, M, et al, editores. Washington (DC): National Academies Press (Estados Unidos); 2003.[1]
- ^ Hersom, Matt. "Aplicación de ionóforos en la dieta de ganado". AN285 Departamento de Animal Sciences. University of Florida IFAS Extension. 14 de marzo de 2013.
- ^ El Consejo Editorial de la New York Times10 de mayo de 2014, El aumento de la resistencia a los antibióticos
- ^ Schneider, K; Garrett, L (19 de junio de 2009). "Uso no terapéutico de antibióticos en agricultura Animal, tasas de resistencia correspondiente y lo que puede ser hecho sobre él". Center for Global Development.
- ^ Hurd HS, Doores S, Hayes D, Mathew A, Maurer J, Silley P, cantante RS, Jones RN (2004). "Consecuencias de salud pública del macrólido usan en alimentación animales: una evaluación de riesgos determinista". J. alimentos Prot. 67 (5): 980 – 92. PMID15151237.
- ^ Hurd HS, Malladi S (2008). "Una evaluación estocástica de los riesgos de salud pública del uso de antibióticos macrólidos en animales de alimentos". Riesgo Anal. 28 (3): 695-710. Doi:10.1111/j.1539-6924.2008.01054.x. PMID18643826.
- ^ Conjunto de la FAO, OIE y OMS experto taller sobre el uso de antimicrobianos no humanos y resistencia a los antimicrobianos: evaluación científica [2]
- ^ OIE, código de Salud Animal terrestre
- ^ OIE, código de Salud Animal terrestre
- ^ OIE, código de Salud Animal terrestre
- ^ Castanon JI (2007). "Historia del uso de antibióticos como promotores del crecimiento en avícola europeo alimenta". Pavipollos. SCI. 86 (11): 2466 – 71. Doi:10.3382/PS.2007-00249. PMID17954599.
- ^ B Bengtsson, Wierup M; Wierup, M. (2006). "Resistencia a los antimicrobianos en Escandinavia tras prohibición de promotores del crecimiento antimicrobianos". Anim Biotechnol. 17 (2): 147 – 56. Doi:10.1080/10495390600956920. PMID17127526.
- ^ "Resistencia antibiótica, GAO-11-801: agencias han realizado progresos limitados abordar el uso de antibióticos en los animales". Gao.gov. 2014-01-25.
- ^ AR Sapkota, Lefferts LY, McKenzie S, Walker P (mayo de 2007). "¿Qué comer a los animales de producción de alimentos? Una revisión de Animal Feed ingredientes y sus impactos potenciales sobre la salud humana". Environ. Salud Perspect. 115 (5): 663 – 70. Doi:10.1289/EHP.9760. PMC1867957. PMID17520050.
- ^ Baker R (2006). "Gestión de la salud con el uso de antibióticos reducido — la experiencia estadounidense". Anim Biotechnol. 17 (2): 195-205. Doi:10.1080/10495390600962274. PMID17127530.
- ^ "Resumen del informe de UCS"acaparando lo: estimaciones de antimicrobianos abuso en ganadería"". La Unión de científicos preocupados. Enero de 2001.
- ^ Nelson JM, Chiller TM, poderes JH, Angulo FJ (abril de 2007). "Especies de Campylobacter Fluoroquinolone-resistente y la retirada de las fluoroquinolonas de uso en las aves de corral: una historia de éxito de la salud pública". Clin infecta Dis 44 (7): 977 – 80. Doi:10.1086/512369. PMID17342653.
- ^ APHIS. "Clostridium difficile sobre las operaciones de Estados Unidos porcina". 24 de octubre de 2013.
- ^ "Senado de Estados Unidos Bill S. 549: preservación de antibióticos para el tratamiento médico Act of 2007".
- ^ "Preservación de antibióticos para tratamiento médico acto de 2007".
- ^ John Gever (23 de marzo de 2012). "FDA dijo que continuar el uso de antibióticos en el ganado". MedPage hoy. 24 de marzo de 2012.
- ^ Gardiner Harris (11 de abril de 2012). "U.S. aprieta las reglas sobre el uso de antibióticos para el ganado". El New York Times. 12 de abril de 2012.
- ^ "Estrategia de la FDA sobre la resistencia a los antimicrobianos: preguntas y respuestas". Administración de drogas y alimentos de Estados Unidos. 11 de abril de 2012. 12 de abril de 2012. ""Uso juicioso"está utilizando un fármaco antimicrobiano apropiadamente y sólo cuando sea necesario; Basado en una revisión exhaustiva de la información científica disponible, la FDA recomienda que el uso de antimicrobianos médicamente importantes productores de alimentos animales se limita a situaciones donde el uso de estos fármacos es necesario para asegurar la salud animal, y su uso incluye supervisión veterinaria o consulta. FDA cree que el uso antimicrobianos médicamente importantes para aumentar la producción en producción de alimentos animales no es un uso juicioso. "
- ^ Tavernise, Sabrina. "La FDA a fase de uso de antibióticos en los animales criados para carne". El New York Times. 11 de diciembre de 2013.
- ^ a b Martinez, J. L. & Olivares, J. (2012). Contaminación medioambiental por los Genes de resistencia a los antibióticos. En P. L. Keen & M. H. Montforts, resistencia a los antimicrobianos en el medio ambiente (pp. 151 - 171). Hoboken, NJ: John Wiley & Sons.
- ^ Pruden, A. & Arabi, M. (2012). Cuantificar los impactos antropogénicos en reservorios ambientales de resistencia a los antibióticos. En P. L. Keen & M. H. Montforts, resistencia a los antimicrobianos en el medio ambiente (pp. 173-202). Hoboken, NJ: John Wiley & Sons.
- ^ OCHIAI, K.; Yamanaka, T; Kimura, K; Sawada, O (1959). "Herencia de la resistencia a los medicamentos (y su transferencia) entre las cepas de Shigella y tensiones entre Shigella y e. coli". Hihon Iji Shimpor, (en japonés) 34:: 1861.
- ^ Li XZ, Nikaido H; Nikadio, H (2009). "Resistencia a las drogas en las bacterias mediada por la emanación: una actualización". Drogas 69 (12): 1555 – 623. Doi:10.2165/11317030-000000000-00000. PMC2847397. PMID19678712.
- ^ Morita Y, Kodama K, Shiota S, mina T, Kataoka A, T Mizushima, Tsuchiya T (julio de 1998). "Norma, una proteína supuesta emanación del Multidrug, Vibrio parahaemolyticus y su homólogo en Escherichia coli". Antimicrob. Agentes Chemother. 42 (7): 1778 – 82. PMC105682. PMID9661020.
- ^ Robicsek A, GA Jacoby, Hooper DC; Jacoby, GA; Hooper, DC (octubre de 2006). "La emergencia mundial de resistencia a quinolonas mediada por plásmidos". Lancet infecta Dis 6 (10): 629 – 40. Doi:10.1016/S1473-3099 (06) 70599-0. PMID17008172.
- ^ Cirz RT, barbilla JK, Andes DR, de Crécy-bibles V, Craig WA, Romesberg FE (2005). "Inhibición de la mutación y la lucha contra la evolución de la resistencia a los antibióticos". PLoS Biol. 3 (6): e176. Doi:10.1371/Journal.pbio.0030176. PMC1088971. PMID15869329.
- ^ Chan CX, Beiko RG, Ragan MA; Beiko, RG; Ragan, MA (agosto de 2011). "Transferencia lateral de Genes y fragmentos génicos de Staphylococcus se extiende más allá de los elementos móviles". J Bacteriol 193 (15): 3964 – 3977. Doi:10.1128/JB.01524-10. PMC3147504. PMID21622749.
- ^ "CDC: Get Smart: saber cuando los antibióticos trabajan". CDC.gov. 2013-06-12.
- ^ "APUA: antecedentes generales: resistencia a los antibióticos, un problema social". Tufts.edu. 2013-06-12.
- ^ B Bozdogan, Esel D, blanqueador C, Browne FA, Appelbaum PC (2003). "Susceptibilidad antibacteriana de una cepa de aureus estafilococo resistente a la vancomicina aislada en el centro médico Hershey". Diario de quimioterapia antimicrobiana 52 (5): 864-868. Doi:10.1093/jac/dkg457. PMID14563898.
- ^ Xie J, Pierce JG, James RC, Okano A Boger DL (2011). "Una rediseñado vancomicina dirigida para doble enlace d-Ala-d-Ala y d-Ala-d-Lac exhibe potente actividad antimicrobiana contra bacterias resistentes a la vancomicina". J am Chem SOC 133, 133 (35): 13946 – 9. Doi:10.1021/ja207142h. PMC3164945. PMID21823662.
- ^ Tsiodras S, oro HS, Sakoulas G, Eliopoulos GM, Wennersten C, L Venkataraman, Moellering RC, Ferraro MJ. "Resistencia a Linezolid en un aislado clínico de Staphylococcus aureus". La revista The Lancet 358 (9277): 207-208. Doi:10.1016/S0140-6736 (01) 05410-1. PMID11476839.
- ^ Boyle-Vavra S, Daum RS; Daum, RS (2007). "Adquirida en la comunidad Staphylococcus aureus meticilino-resistente: el papel de Panton-Valentine leukocidin". Laboratorio invertir. 87 (1): 3 – 9. Doi:10.1038/labinvest.3700501. PMID17146447.
- ^ Maree CL, Daum RS, Boyle-Vavra S, K Matayoshi, Miller LG (2007). "Comunidad-associated Methicillin-resistant Staphylococcus aureus aislados y las infecciones intrahospitalarias". Infectan a los emergentes. Dis. 13 (2): 236 – 42. Doi:10.3201/eid1302.060781. PMC2725868. PMID17479885.
- ^ CDCP (2005-10-11). "Enfermedad de (GAS) por estreptococo grupo A (estreptococo garganta, necrosante, fascitis, impétigo)--preguntas frecuentes". Centers for Disease Control and Prevention. Programa archivado de la original en 19 de diciembre de 2007. de 2007-12-11.
- ^ a b Albrich WC, Monnet DL, Harbarth S; Monnet, DL; Harbarth, S (2004). "Presión de selección de antibióticos y resistencia en Streptococcus pneumoniae y Streptococcus pyogenes". Infectan a los emergentes. Dis. 10 (3): 514 – 7. Doi:10.3201/eid1003.030252. PMC3322805. PMID15109426.
- ^ Hidron AI, Edwards JR, J Patel, Horan TC, Sievert DM, Pollock DA, Fridkin SK (noviembre de 2008). "Actualización anual NHSN: patógenos resistentes a los antimicrobianos asociados con infecciones relacionadas con la salud: Resumen anual de los datos registrados a la red nacional de seguridad sanitaria de los centros para el Control de enfermedades y prevención, 2006-2007". Control Hosp Epidemiol infectar 29 (11): 996 – 1011. Doi:10.1086/591861. PMID18947320.
- ^ Poole K (2004). "Mediada por la emanación multirresistencia en bacterias Gram-negativas". Infección y microbiología clínica 10 (1): 12 – 26. Doi:10.1111/j.1469-0691.2004.00763.x. PMID14706082.
- ^ D Nguyen, Joshi-Datar A, F Lepine, Bauerle E, Olakanmi O, cerveza K, McKay G, Siehnel R, Schafhauser J, Wang Y, Britigan ser, Singh PK (2011). "Hambre activa respuestas median antibiótica tolerancia en Biofilms y bacterias de nutrientes limitados". Ciencia 334 (6058): 982 – 6. Doi:10.1126/science.1211037. PMID22096200.
- ^ Gerding DN, Johnson S, Peterson LR, ME Mulligan, Silva J (1995). "Clostridium difficile-asociada diarrea y colitis". Infectar. Control. Hospital Epidemiol. 16 (8): 459-477. Doi:10.1086/648363. PMID7594392.
- ^ McDonald ' s LC (2005). "El Clostridium difficile:: respondiendo a una nueva amenaza de un viejo enemigo ". Infectar. Control. Hospital Epidemiol. 26 (8): 672 – 5. Doi:10.1086/502600. PMID16156321.
- ^ Baxter R, Ray GT, bombero BH (enero de 2008). "Estudio de casos y controles de uso de antibióticos y posterior diarrea difficile-asociada del Clostridium en pacientes hospitalizados". Control de infecciones y epidemiología hospitalaria: el diario oficial de la sociedad de Epidemiología del Hospital de América 29 (1): 44 – 50. Doi:10.1086/524320. PMID18171186.
- ^ Gifford, Kirkland KB (diciembre de 2006). "Factores de riesgo para la diarrea del Clostridium difficile-asociada en una sala de adultos hemato-oncología". Diario europeo de microbiología clínica y enfermedades infecciosas: publicación oficial de la sociedad europea de microbiología clínica 25 (12): 751 – 5. Doi:10.1007/s10096-006-0220-1. PMID17072575.
- ^ TN Palmore, S Sohn, Malak SF, Eagan J, Sepkowitz KA (agosto de 2005). "Factores de riesgo para la adquisición de Clostridium difficile-diarrea asociada con antibióticos entre pacientes ambulatorios en un hospital de cáncer". Control de infecciones y epidemiología hospitalaria: el diario oficial de la sociedad de Epidemiología del Hospital de América 26 (8): 680 – 4. Doi:10.1086/502602. PMID16156323.
- ^ Johnson S, Samore MH, Farrow KA, Killgore GE, Tenover FC, Lyras D, Rood JI, DeGirolami P, Baltch AL, ME Rafferty, pera SM, Gerding DN (1999). "Las epidemias de diarrea causada por una cepa resistente a clindamicina de El Clostridium difficile en cuatro hospitales". New England Journal of Medicine 341 (23): 1645 – 1651. Doi:10.1056/NEJM199911253412203. PMID10572152.
- ^ Loo VG, Poirier L, Miller MA, Oughton M, Libman MD, S Michaud, Bourgault AM, Nguyen T, C Frenette, Kelly M, Vibien A, Brassard P, S Fenn, Dewar K, Hudson TJ, cuerno R, René P, Monczak Y Dascal A (2005). "Un brote multi-institucional predominante clonal de diarrea del Clostridium difficile-asociada con alta morbilidad y mortalidad". N Engl J Med 353 (23): 2442 – 9. Doi:10.1056/NEJMoa051639. PMID16322602.
- ^ "Acinetobacter baumannii infecciones entre los pacientes en las instalaciones médicas militares tratar heridos miembros del servicio de Estados Unidos, 2002-2004". MMWR Morb. Mortal. Wkly. Rep. (Centers for Disease Control and Prevention (CDC)) 53 (45): 1063 – 6. 2004. PMID15549020.
- ^ "Resumen de Medscape Acinetobacter baumannii: Acinetobacter baumannii: An Emerging multirresistente amenaza". "sitio Web única pertenencia"
- ^ Hudson, Corey; Bent, Zachary; Meagher, Robert; Williams, Kelly (07 de junio de 2014). "Determinantes de resistencia y elementos genéticos móviles de un NDM-1-Encoding Klebsiella pneumoniae cepa". PLoS uno. Doi:10.1371/Journal.pone.0099209.
- ^ Arnold RS, Thom KA, Sharma S, Phillips M, Kristie Johnson J, Morgan DJ (2011). "Aparición de Klebsiella pneumoniae Carbapenemase-produciendo bacterias". Southern Medical Journal 104 (1): 40 – 5. Doi:10.1097/SMJ.0b013e3181fd7d5a. PMC3075864. PMID21119555.
- ^ "Resistencia a los antimicrobianos aún representa una amenaza de salud pública: una conversación con Edward J. Septimus, MD, FIDSA, FACP, FSHEA, profesor clínico de medicina interna en Texas A & M Health Science Center". Agency for Healthcare Research and Quality. 17 / 04 / 2013. 26 / 09 / 2013 obtenido.
- ^ a b LoBue P (2009). "La tuberculosis extremadamente farmacorresistente." Opinión actual de las enfermedades infecciosas 22 (2): 167 – 73. Doi:10.1097/QCO.0b013e3283229fab. PMID19283912.
- ^ Herzog H (1998). "Historia de la Tuberculosis". Respiración 65 (1): 5 – 15. Doi:10.1159/000029220. PMID9523361.
- ^ Gao, Qian; Li, Xia (2010). "La transmisión de la tuberculosis multirresistente". Hoy el descubrimiento de fármacos: Mecanismos de la enfermedad 7:: e61. Doi:10.1016/j.ddmec.2010.09.006.
- ^ Ligon, B. Lee (octubre de 2005). "Albert Ludwig Sigesmund Neisser: descubridor de la causa de la gonorrea". Seminarios en enfermedades infecciosas pediátricas 16 (4): 336-341. Doi:10.1053/j.SPID.2005.07.001.
- ^ Rosner, Fred (1995). Medicina en la Biblia y el Talmud: selecciones de fuentes judías clásicas (Augm. ed. ed.). Hoboken, NJ: KTAV Pub. Casa. ISBN0-88125-506-8.
- ^ a b Resistencia a los antimicrobianos en Tapsall (2001) Neisseria gonorrhoeae. Organización Mundial de la salud.
- ^ T Deguchi, Nakane K, Yasuda M, Maeda S (septiembre de 2010). Aparición y propagación de Neisseria gonorrhoeae resistentes a los fármaco. J. urol. 184 (3): 851 – 8; el concurso 1235. Doi:10.1016/j.juro.2010.04.078. PMID20643433.
- ^ "Actualización de las pautas de tratamiento de enfermedades transmitidas sexualmente de los CDC, 2010: cefalosporinas orales ya No es un tratamiento recomendado para infecciones gonocócicas.". MMWR. Informe semanal de morbilidad y mortalidad 61 (31): 590 – 4. 10 de agosto de 2012. PMID22874837.
- ^ "Evolución de la resistencia a los antibióticos". PBS.org. WGBH Educational Foundation y Clear Blue Sky Productions, Inc. 11 de junio de 2013.
- ^ ME McCusker, Harris AD, Perencevich E, Roghmann MC (2003). "Uso de fluoroquinolonas y Clostridium difficile – Associated diarrea". Infectan a los emergentes. Dis. 9 (6): 730 – 3. Doi:10.3201/eid0906.020385. PMC3000134. PMID12781017.
- ^ Helada F, Craun GF, Calderon RL; Craun, GF; Calderon, RL (1998). "Aumento de hospitalización y muerte posiblemente debido a la enfermedad diarreica Clostridium difficile". Infectan a los emergentes. Dis. 4 (4): 619-25. Doi:10.3201/eid0404.980412. PMC2640242. PMID9866738.
- ^ "Inmunidad, enfermedades infecciosas y las pandemias — lo que puede hacer". HomesteadSchools.com. 2013-06-12.
- ^ a b "Ciencia, tecnología, genética, investigación sobre biotecnología: diciembre 2009". Biotechnolo.blogspot.com. 2013-06-12.
- ^ CE agudo (2012). "La terapia phage: concepto de curar". Microbiol frontal 3:: 238. Doi:10.3389/fmicb.2012.00238. PMC3400130. PMID22833738.
- ^ Chanishvili, N; Chanishvili, T; Tediashvili, M.; Barrow, P.A. (2001). "Phages y su aplicación contra bacterias resistentes a los medicamentos". J Chem Technol Biotechnol. 76 (7): 689-699. Doi:10.1002/jctb.438.
- ^ Jikia D, Chkhaidze N, Imedashvili E, Mgaloblishvili I, Tsitlanadze G, Katsarava R, Glenn Morris J, Sulakvelidze A (2005). "El uso de una preparación biodegradable novela capaz de la liberación sostenida de bacteriófagos y ciprofloxacina, en el tratamiento complejo de multidrug-resistant Staphylococcus aureus-infectados local radiolesiones causada por exposición al Sr90". Dermatología clínica y Experimental 30 (1): 23 – 6. Doi:10.1111/j.1365-2230.2004.01600.x. PMID15663496.
- ^ B Weber-Dabrowska, Mulczyk M, Górski (junio de 2003). "Bacteriófagos como una terapia eficaz para septicemia resistentes a los antibióticos en el hombre". Trasplante. Proc. 35 (4): 1385 – 6. Doi:10.1016/S0041-1345 (03) 00525 6. PMID12826166.
- ^ Chowdhry S, Pandhi D, Vidhani S, Bhalla P, Reddy BS (2003). "La terapia bacteriófago: una alternativa a los antibióticos convencionales". J Assoc Physicians India 51 (8): 593 – 6. Doi:10.1258/095646202760159701. PMID12194741.
- ^ Los científicos descubren alternativa posible antibióticos -Australian Broadcasting Corporation — obtenido 29 de julio de 2012.
- ^ Informe anual CMO
- ^ a b La administración Obama pretende facilitar aprobaciones de antibióticos: Disparos - noticias de salud: NPR
- ^ Moldavia lucha ya sea aislar a los pacientes de TB: NPR
- ^ a b Walsh, Fergus. "Noticias de BBC, resistencia a antibióticos 'tan arriesgado como terrorismo' - jefe médico". BBC.co.uk. 2013-03-12.
- ^ Gever, John (2011-02-04). "Pfizer movimientos pueden tenue posibilidad para nuevos antibióticos". MedPage hoy. 2013-03-12.
- ^ Ledford H (2012). "La FDA bajo presión para relajar las reglas de la droga". Naturaleza 492 (7427): 19. Doi:10.1038/492019a. PMID23222585.
- ^ Comunicado de prensa (12 de diciembre de 2013). "Verde, Gingrey introducir adaptar la ley para salvaguardar la salud pública". Congreso de Estados Unidos.
- ^ "Desarrollo de antibiótico para promover ley de tratamiento de los pacientes de 2013". Congreso de Estados Unidos. 12 de diciembre de 2013.
- ^ NIH a fondo la red de investigación clínica sobre la resistencia antibacteriana
- ^ PHE
- ^ Mukhopadhyay J, K Das, Ismail S, Koppstein D, Jang M, Hudson B, Sarafianos S, Tuske S, Patel J, Jansen R, H Irschick, Arnold E, Ebright RH (2008). "La polimerasa del RNA"región del conmutador"es un objetivo para los inhibidores". Celular 135 (2): 295-307. Doi:10.1016/j.Cell.2008.09.033. PMC2580802. PMID18957204.
- ^ "Abeja modificado péptido mata a las bacterias mortales | Chemical & Engineering News". 29-05-2012 CEN.ACS.org.. 2013-03-12.
- ^ Ponte-Sucre, A, ed. (2009). Transportadores ABC en microorganismos. Caister Academic Press. ISBN978-1-904455-49-3.[Página necesitado]
Referencias
- Libros
- Caldwell, Roy; Lindberg, David, eds (2011). "Evolución de la comprensión" [las mutaciones son al azar]. Museo de Paleontología de la Universidad de California. 14 de agosto de 2011.
- Nelson, Richard William (2009). Darwin, entonces y ahora: la historia más increíble de la historia de la ciencia (Auto publicado). iUniverse. p. 294.
- Revistas
- Arias CA, Murray ser; Murray, ser (2009). "Los insectos resistentes a los antibióticos en el siglo XXI — un desafío súper clínico". New England Journal of Medicine 360 (5): 439-443. Doi:10.1056/NEJMp0804651. PMID19179312.
- D'Costa, Vanessa; King, Christine; Kalan, Lindsay; Morar, Mariya; Sung, Wilson; Schwarz, Carsten; Froese, Duane; Zazula, Grant; Calmels, Fabrice; Debruyne, Regis; Golding, Brian G.; Poinar, Hendrik N.; Wright, D. Gerard (septiembre de 2011). "Resistencia a los antibióticos es antigua". Naturaleza 477 (7365): 457-461. Bibcode:2011Natur.477...D 457. Doi:10.1038/nature10388. PMID21881561.
- Donadio, Stefano; Maffioli, Sonia; Monciardini, Paolo; Sosio, Margherita; Jabes, Daniela (agosto de 2010). "Descubrimiento de antibiótico en el siglo XXI: tendencias actuales y perspectivas futuras". El diario de los antibióticos 63 (8): 423-430. Doi:10.1038/ja.2010.62. PMID20551985.
- Goossens H, Ferech M, Vander Stichele R, Elseviers M; Ferech, M; Vander Stichele, R; Elseviers, M; Proyecto ESAC, grupo (2005). "El uso de antibióticos para pacientes ambulatorios en Europa y en asociación con resistencia: un estudio de base de datos transnacionales". The Lancet. Grupo proyecto Esac 365 (9459): 579 – 87. Doi:10.1016/S0140-6736 (05) 17907-0. PMID15708101.
- Hawkey, PM; Jones, AM (septiembre de 2009). "La epidemiología cambiante de la resistencia". El diario de la quimioterapia antimicrobiana. 64 Suppl 1: i3 – 10. Doi:10.1093/jac/dkp256. PMID19675017.
- Soulsby EJ (2005). "Resistencia a los antimicrobianos en los seres humanos y animales: el uso excesivo de antibióticos no es la única causa y reducir el uso no es la única solución". British Medical Journal 331 (7527): 1219 – 20. Doi:10.1136/bmj.331.7527.1219. PMC1289307. PMID16308360.
- "Alternativas a los antibióticos reducen la enfermedad Animal". Organización de investigación científica e Industrial de Commonwealth. 09 de enero de 2006.
Enlaces externos
- Animación de resistencia a los antibióticos
- Artículo de CDC en Hospital adquirió MRSA
- Artículo de CDC sobre comunidad adquirió MRSA
- Pauta del CDC "Gestión de los organismos multirresistentes en entornos sanitarios, 2006"
- Reaccionar acción sobre resistencia a los antibióticos
- Alianza para el uso prudente de antibióticos
- LA Cox, Popken DA (2006). "Cuantificar los impactos potenciales de Salud Animal del uso de antibióticos: Enrofloxacina y macrólidos en los pollos". Análisis de riesgos 26 (1): 135-146. Doi:10.1111/j.1539-6924.2006.00723.x. PMID16492187.
- Información sobre terapia phage – una posible alternativa a los antibióticos en caso de infecciones resistentes a
- Genes de resistencia a antibióticos como marcadores Una vez necesario, ahora indeseable
- CBS artículo sobre terapia Phage y resistencia a los antibióticos
- Hospitales: Cría la superbacteria Artículo sobre infecciones MRSA en los hospitales, conocimiento de Allianz, por deseo de Valdis, mayo de 2008.
- CARGA de resistencia y de la enfermedad en las naciones europeas - un proyecto de la UE para estimar la carga financiera de resistencia a los antibióticos en los hospitales europeos
- Extendiendo la curación: la investigación de políticas para ampliar la eficacia antibiótica
- 2003 nueva orientación para la industria en antimicrobiano drogas para alimentos animales preguntas y respuestas, los E.E.U.U. FDA
- Foco de resistencia de SciDev.net antibiótico El Science and Development Network es una red de desarrollo centrado en noticias e información importante para el mundo en desarrollo y ciencia en línea
- ¿Bugs necesita drogas?
- La lucha contra la resistencia a los medicamentos -Lucha contra la resistencia a las drogas en las bacterias y otros agentes patógenos.
- [3] Las nanopartículas podrían tratar las infecciones resistentes a los antibióticos.
|
||||||||||||||||||||||||||
Otras Páginas
- Universidad Americana de Orgonomy
- Dispositivo de asistencia ventricular
- Estrategia de inversion basada en la responsabilidad
- Referendum de la creacion de Nunavut, 1992
- Lista de tipos de registros DNS
- Ruta Estatal de Nevada 51 (1960s)
- Namespace global
- Bomba de calabaza
- Iniciativa de pago abierto
- Mike Edmonson
- Restriccion historica analisis genomico
- Theraplay
- Beatbullyz