Cáncer de pulmón
| Cáncer de pulmón | |
|---|---|

A radiografía de tórax que muestra un tumor en el pulmón (señalado con flecha)
|
|
| Clasificación y recursos externos | |
| Especialidad | Oncología |
| ICD-10 | C33-C34 |
| ICD-9-CM | 162 |
| OMIM | 211980 |
| DiseasesDB | 7616 |
| MedlinePlus | 007194 |
| eMedicine | Med/1333 Med/1336 emerg/335 radio/807 radio/405 radio/406 |
| Paciente Reino Unido | Cáncer de pulmón |
| Malla | D002283 |
Cáncer de pulmón, también conocido como carcinoma del pulmón o carcinoma pulmonar, es un malo tumor del pulmón caracteriza por descontrolado crecimiento de la célula en tejidos de la pulmón. Si no se trata, este crecimiento puede propagarse más allá de los pulmones por el proceso de metástasis en los tejidos circundantes o de otras partes del cuerpo. La mayor parte cánceres de que empiezan en los pulmones, conocido como los cánceres de pulmón primarios, son carcinomas que se derivan de epiteliales células. Los principales tipos primarios son carcinoma de pulmón de células pequeñas (SCLC) y carcinoma de pulmón de células no pequeñas (CPCNP). Los más comunes síntomas son tos (incluyendo expectoración con sangre), pérdida de peso, dificultad para respirar y dolores en el pecho.[1]
La gran mayoría (80-90%) de casos de cáncer de pulmón es debido a la exposición a largo plazo a el humo del tabaco.[1][2] 10 – 15% de los casos ocurren en personas que nunca han fumado.[3] Estos casos son causados a menudo por una combinación de factores genéticos[4] y la exposición a radón gas,[4] amianto,[5] u otras formas de contaminación del aire,[4] incluyendo humo de segunda mano.[6][7] Cáncer de pulmón puede verse en radiografías de pecho y tomografía computada (TC). El diagnóstico se confirma por biopsia de la[8] que se realiza generalmente por Broncoscopia o dirección de CT.
Tratamiento y resultados a largo plazo dependen del tipo de cáncer, la etapa (grado de propagación) y la salud general de la persona, medido por Estado de rendimiento. Los tratamientos comunes incluyen cirugía, quimioterapia, y radioterapia. NSCLC a veces se trata con cirugía, mientras que SCLC generalmente responde mejor a la quimioterapia y radioterapia.[9] General, 16.8% de personas en los Estados Unidos diagnosticados con cáncer de pulmón sobreviven cinco años Tras el diagnóstico,[10] mientras que los resultados en promedio son peores en el mundo en desarrollo. En todo el mundo, cáncer de pulmón es la causa más común de muerte relacionada con cáncer en hombres y mujeres y fue responsable de 1,56 millones de muertes anualmente, a partir de 2012.[11]
Contenido
- 1 Signos y síntomas
- 2 Causas
- 2.1 Fumar
- 2.2 Gas radón
- 2.3 Amianto
- 2.4 Contaminación del aire
- 2.5 Genética
- 2.6 Otras causas
- 3 Patogénesis
- 4 Diagnóstico
- 4.1 Clasificación
- 4.1.1 Carcinoma del pulmón de células no pequeñas
- 4.1.2 Carcinoma de pulmón de células pequeñas
- 4.1.3 Otros
- 4.2 Metástasis
- 4.3 Puesta en escena
- 4.1 Clasificación
- 5 Prevención
- 5.1 Prohibición de fumar
- 5.2 Proyección
- 5.3 Otras estrategias de prevención
- 6 Gestión
- 6.1 Cirugía
- 6.2 Radioterapia
- 6.3 Quimioterapia
- 6.3.1 Terapia dirigida
- 6.4 Cuidados paliativos
- 7 Pronóstico
- 8 Epidemiología
- 9 Historia
- 10 Direcciones de investigación
- 11 Referencias
- 12 Acoplamientos externos
Signos y síntomas
Signos y síntomas que puedan sugerir cáncer de pulmón incluyen:[1]
- Síntomas respiratorios: tos, expectoración con sangre, sibilancias o dificultad para respirar
- Síntomas sistémicos: pérdida de peso, fiebre, Clubbing de las uñas, o fatiga
- Síntomas debido a la masa de cáncer presionando sobre las estructuras adyacentes: dolor en el pecho, dolor óseo, obstrucción de vena cava superior, dificultad para deglutir
Si el cáncer crece en el vías respiratorias, puede obstruir la circulación de aire, causando dificultad para respirar. La obstrucción puede conducir a acumulación de secreciones detrás de la obstrucción y predisponen a la neumonía.[1]
Dependiendo del tipo de tumor, fenómenos paraneoplásicos— los síntomas no debidos a la presencia local de cáncer, inicialmente puede atraer la atención a la enfermedad.[12] En cáncer de pulmón, estos fenómenos pueden incluir Síndrome miasténico de Lambert-Eaton (debilidad del músculo debido a autoanticuerpos), hipercalcemia, o síndrome de hormona antidiurética (SIADH, orina anormalmente concentrada y diluida). Tumores en la parte superior del pulmón, conocido como Tumores de Pancoast, puede invadir la parte local de la sistema nervioso simpático, llevando a Síndrome de Horner (caída del párpado y una pupila pequeña de ese lado), así como daños a la del plexo braquial.[1]
Muchos de los síntomas del cáncer de pulmón (falta de apetito, pérdida de peso, fiebre, fatiga) no son específicos.[8] En muchas personas, el cáncer ya se ha diseminado más allá del sitio original en el momento en tiene síntomas y busque atención médica.[13] Síntomas que sugieren la presencia de enfermedad metastásica incluyen pérdida de peso, dolor de huesos y síntomas neurológicos (dolores de cabeza, desmayo, convulsioneso debilidad de las extremidades).[1] Sitios comunes de propagación incluyen el cerebro, hueso, glándulas suprarrenales, otro pulmón, hígado, pericardio, y riñones.[13] Cerca de 10% de las personas con cáncer de pulmón no tienen síntomas en el diagnóstico; estos cánceres se encuentran incidentalmente en la radiografía del pecho rutinaria.[14]
Causas

El cáncer desarrolla después de daño genético a DNA y cambios epigenéticos. Estos cambios afectan las funciones normales de la célula, incluyendo proliferación celular, () muerte celular programadaapoptosis) y la reparación del ADN. Mientras más daño se acumula, aumenta el riesgo de cáncer.[15]
Fumar

Fumar, particularmente de cigarrillos, es de lejos el principal contribuyente al cáncer de pulmón.[16] El humo del cigarrillo contiene por lo menos 73 conocido agentes carcinógenos,[17] incluyendo benzo [a] pireno,[18] NNK, 1, 3-butadieno y un isótopo radiactivo de Polonio, Polonio-210.[17] En todo el mundo desarrollado, el 90% de las muertes por cáncer del pulmón en los hombres durante el año 2000 fueron atribuido a fumar (70% para las mujeres).[19] Fumar representa el 80-90% de casos de cáncer de pulmón.[1]
Tabaquismo pasivo-la inhalación del humo de otros fuma, es una causa de cáncer de pulmón en no fumadores. Un fumador pasivo puede definirse como alguien viven o trabajan con fumadores. Estudios de los Estados Unidos,[20][21][22] Europa[23] y el Reino Unido[24] han demostrado un riesgo significativamente mayor entre aquellos expuestos al humo pasivo.[25] Los que viven con alguien que fuma tiene un 20-30% de aumento en riesgo mientras que los que trabajan en un ambiente con humo de segunda mano tienen un 16-19% aumentan de riesgo.[26] Investigaciones de humo lateral sugieren que es más peligroso que el humo directo.[27] Tabaquismo pasivo causa aproximadamente 3.400 muertes por cáncer de pulmón cada año en los Estados Unidos.[22]
Humo de marihuana contiene muchos de los carcinógenos mismo que en el humo de tabaco.[28] Sin embargo el efecto del tabaquismo cannabis en cáncer de pulmón el riesgo no está claro.[29][30] Una revisión de 2013 no se encontró un mayor riesgo de la luz para moderar el uso.[31] Una revisión de 2014 encontró que cannabis fumar duplica el riesgo de cáncer de pulmón.[32]
Gas radón
Radón es un incoloro e inodoro gas generados por la descomposición de radiactivos radio, que a su vez es el producto de decaimiento de uranio, se encuentran en la tierra corteza. Los productos del decaimiento de la radiación ionizar material genético, causando mutaciones que a veces se hacen cancerosas. El radón es la segunda causa común del cáncer de pulmón en los Estados Unidos,[33] causando unos 21.000 muertes cada año.[34] El riesgo aumenta de 8 a 16% por cada 100 Bq/³ de m aumento en la concentración de radón.[35] Niveles de gas radón varían según la localidad y la composición de los suelos y rocas subyacentes. Aproximadamente uno en 15 casas en los Estados Unidos tiene niveles de radón por encima de la pauta recomendada de 4 picocurios por litro (pCi/l) (148 Bq/m³).[36]
Amianto
Amianto puede causar una variedad de enfermedades pulmonares, incluyendo cáncer de pulmón. Tabaco tabaquismo y el asbesto tienen un sinérgica efecto sobre la formación del cáncer de pulmón.[5] En los fumadores que trabajan con el asbesto, el riesgo de cáncer de pulmón se incrementa 45-fold en comparación con la población en general.[37] Asbesto puede causar también cáncer de la pleura, llamado mesotelioma (que es diferente del cáncer de pulmón).[38]
Contaminación del aire
Contaminación del aire exterior tiene un pequeño efecto en aumentar el riesgo de cáncer de pulmón.[4] Bellas partículas (PM2.5) y aerosoles de sulfato, que se pueden liberar en tráfico de gases del escape, se asocian con riesgo levemente creciente.[4][39] Para dióxido de nitrógeno, un aumento incremental de 10 partes por mil millones aumenta el riesgo de cáncer de pulmón en un 14%.[40] Contaminación atmosférica se estima que son responsables de 1 – 2% de los cánceres de pulmón.[4]
La evidencia tentativa apoya un aumento del riesgo de cáncer de pulmón de contaminación del aire interior relacionadas con la quema de madera, carbón, residuos de estiércol o cultivo para cocinar y calentarse.[41] Las mujeres que están expuestas al humo de carbón interior tienen el doble de riesgo y un número de los subproductos de la quema biomasa se sabe o se sospecha carcinógenos.[42] Este riesgo afecta a unos 2,4 billones de personas a nivel mundial,[41] y se cree que representan el 1,5% de las muertes por cáncer pulmonar.[42]
Genética
Aproximadamente el 8% de cáncer de pulmón es debido a heredado factores.[43] En familiares de personas con cáncer de pulmón, el riesgo aumenta 2,4 veces. Esto es probable debido a un combinación de genes.[44] Polimorfismos de en los cromosomas 5, 6 y 15 se sabe que afectan el riesgo de cáncer de pulmón.[45]
Otras causas
Muchas otras sustancias, ocupaciones y exposición a riesgos ambientales se han relacionado con cáncer de pulmón. El Agencia Internacional de investigación sobre el cáncer (IARC) señala que hay "pruebas suficientes" para demostrar que son cancerígenos en los pulmones:[46]
- Algunos metales (producción de aluminio, cadmio y compuestos de cadmio, cromo(VI) compuestos, berilio y compuestos de berilio, hierro y acero Fundación, compuestos de níquel arsénico y compuestos inorgánicos de arsénico, metro Hematites explotación minera)
- Algunos productos de la combustión (combustión incompleta, carbón (interior emisiones de la quema de carbón doméstico), carbón, brea de alquitrán de carbón, la gasificación producción de coquehollín, gases de escape motor diesel)
- Radiación ionizante (radiación x, radiación gamma, plutonio)
- Algunos gases tóxicos (éter metílico (grado técnico), éter de Bis-(chloromethyl), mostaza de azufre, (MOPPmezcla de mostaza-procarbazina vincristina prednisona de nitrógeno), los vapores de la pintura)
- Producción de caucho y cristalino polvo de sílice
Patogénesis

Similar a muchos otros cánceres, el cáncer de pulmón se inicia por la activación de oncogenes o inactivación de genes supresores de tumores.[47] Agentes carcinógenos causan mutaciones en estos genes que inducen el desarrollo del cáncer.[48]
Mutaciones En K-ras proto-oncogene es responsable de 10 – 30% de los adenocarcinomas de pulmón.[49][50] Aproximadamente el 4% de los carcinomas de pulmón de células no pequeñas implican un EML4-ALK cinasa de la tirosina gen de fusión.[51]
Epigenéticos cambios, tales como alteración de Metilación del ADN, histonas modificación, la cola o microRNA regulación, puede llevar a la inactivación de genes supresores de tumores.[52]
El receptor del factor de crecimiento epidérmico (EGFR) regula la proliferación celular, apoptosis, angiogénesisy la invasión del tumor.[49] Las mutaciones y la amplificación de EGFR son comunes en el carcinoma de pulmón de células no pequeñas y proporcionan la base para el tratamiento con inhibidores del EGFR. HER2/neu se afecta con menos frecuencia.[49] Otros genes mutados o amplificados a menudo son c-MET, NKX2-1, LKB1, PIK3CA, y BRAF.[49]
Las líneas celulares de origen no se entienden completamente.[1] El mecanismo puede implicar una activación anormal de células madre. En las vías respiratorias proximales, las células que expresan de la madre queratina 5 son más propensos a ser afectados, típicamente conduce a carcinoma del pulmón de células escamosas. En las vías respiratorias medias, células implicadas incluyen células del Club y células neuroepiteliales express proteína secretora de la célula de Club. Carcinoma de pulmón de células pequeñas puede derivarse de estas líneas celulares[53] o células neuroendocrinas,[1] y puede expresar CD44.[53]
Metástasis de cáncer de pulmón requiere transición de epitelial a mesenquimales tipo de la célula. Esto puede ocurrir a través de la activación de vías de señalización como Akt/GSK3Beta, MEK-ERK, FASy Par6.[54]
Diagnóstico

Realización de un radiografía de tórax es uno de los primeros pasos de la investigación, si una persona informa de síntomas que pueden sugerir cáncer de pulmón. Esto puede revelar una masa obvia, ampliación de la mediastino (sugestivos de diseminación a los ganglios linfáticos allí), atelectasia (colapso), consolidación (neumonía) o derrame pleural.[2] Proyección de imagen de CT se suele utilizar para proporcionar más información acerca del tipo y extensión de la enfermedad. Broncoscopia o guiada por TC biopsia de la a menudo se utiliza para la muestra del tumor para histopatología.[14]
Cáncer de pulmón a menudo aparece como un nódulo pulmonar solitario en una radiografía de tórax. Sin embargo, la Diagnóstico diferencial es amplia. Muchas otras enfermedades también pueden dar este aspecto, incluyendo tuberculosis, micosis, cáncer metastásico o pulmonía de organización. Son causas menos comunes de un nódulo pulmonar solitario amartomas, quistes broncogénicos, adenomas, malformación arteriovenosa, secuestro pulmonar, nódulos reumatoides, s con poliangeítis, o linfoma.[55] Cáncer de pulmón también puede ser un encontrar fortuito, como un nódulo pulmonar solitario en una radiografía de tórax o una tomografía computarizada hecha por una razón sin relación.[56] El diagnóstico definitivo de cáncer de pulmón se basa en histológicos examen del tejido sospechoso en el contexto de las características clínicas y radiológicas.[1]
Guías de práctica clínica Recomendamos las frecuencias para pulmonar nódulo vigilancia.[57] Proyección de imagen de CT no debería utilizarse por más tiempo o más con frecuencia que la indicada como extendido vigilancia expone a las personas a la radiación mayor.[57]
Clasificación
| Tipo histológico | Incidencia por 100.000 por año |
|---|---|
| Todos los tipos | 66.9 |
| Adenocarcinoma | 22.1 |
| Carcinoma de la squamous-célula | 14.4 |
| Carcinoma de células pequeñas | ArgumentException: The incoming token has expired. Get a new access token from the Authorization Server. : ID=5005.V2_Json.Translate.1A42C422 |
Los cánceres de pulmón se clasifican según tipo histológico.[8] Esta clasificación es importante para determinar la gestión y predicción de los resultados de la enfermedad. Los cánceres de pulmón son carcinomas— neoplasias malignas que surgen de células epiteliales. Carcinomas de pulmón se clasifican por el tamaño y la apariencia de las células malignas por histopathologist debajo de un microscopio. Para fines terapéuticos, se distinguen dos grandes clases: carcinoma de pulmón de células no pequeñas y carcinoma de pulmón de células pequeñas.[58]
Carcinoma del pulmón de células no pequeñas

Los tres subtipos principales de CPCNP son adenocarcinoma, carcinoma de células escamosas y carcinoma de células grandes.[1]
Casi el 40% de los cánceres de pulmón son adenocarcinoma, que generalmente se origina en tejido pulmonar periférico.[8] Aunque la mayoría de los casos de adenocarcinoma se asocian con el tabaquismo, adenocarcinoma también es la forma más común de cáncer de pulmón entre personas que han fumado menos de 100 cigarrillos en su vida ("no fumadores").[1][59] Un subtipo de adenocarcinoma, el carcinoma de bronchioloalveolar, es más común en mujeres no fumadoras y pueden tener una supervivencia mejor a largo plazo.[60]
Carcinoma de células escamosas representa alrededor del 30% de cánceres de pulmón. Se producen típicamente cerca vías aéreas grandes. A hueco cavidad y asociados muerte de la célula se encuentran comúnmente en el centro del tumor.[8] Alrededor del 9% de los cánceres de pulmón son carcinoma de células grandes. Estos se llaman así porque las células cancerosas son grandes, con exceso citoplasma, grandes núcleos y llamativo nucleolos.[8]
Carcinoma de pulmón de células pequeñas

En carcinoma de pulmón de células pequeñas (SCLC), las células contienen gránulos neurosecretory densos (vesículas que contiene neuroendocrino hormonas), que dan a este tumor una asociación de síndrome endocrino, paraneoplásico.[61] Mayoría de los casos se presenta en las vías respiratorias más grandes (primarias y secundarias bronquios).[14] Estos cánceres crecen rápidamente y difundir temprano en el curso de la enfermedad. Sesenta a setenta por ciento enfermedad metastásica en la presentación. Este tipo de cáncer de pulmón está fuertemente asociado con el tabaquismo.[1]
Otros
Se reconocen cuatro subtipos histológicos principales, aunque algunos tipos de cáncer pueden contener una combinación de diferentes subtipos.[58] Los subtipos raros incluyen tumores glandulares, tumores carcinoidesy undifferentiated carcinomas.[1]
Metástasis
| Tipo histológico | Immunostain |
|---|---|
| Carcinoma de la squamous-célula | CK5/6 positiva CK7 negativo |
| Adenocarcinoma | CK7 positivo TTF-1 positiva |
| Carcinoma de células grandes | TTF-1 negativo |
| Carcinoma de células pequeñas | TTF-1 positivo CD56 positiva Chromogranin positiva Synaptophysin positiva |
El pulmón es un lugar común para la propagación de tumores de otras partes del cuerpo. Cáncer secundario se clasifica por sitio de origen; por ejemplo, el cáncer de mama que se ha propagado al pulmón se llama cáncer de mama metastásico. Las metástasis a menudo han una característica aspecto en la radiografía de tórax.[62]
Los cánceres de pulmón primarios ellos mismos comúnmente hacen metástasis al cerebro, huesos, hígado y glándulas suprarrenales.[8] Inmunotinción de una biopsia a menudo es útil para determinar la fuente original.[63]
Puesta en escena
Pulmón Estadificación del cáncer es una evaluación del grado de diseminación del cáncer desde su fuente original. Es uno de los factores que afectan la pronóstico y tratamiento potencial del cáncer de pulmón.[1]
La evaluación inicial de carcinoma de pulmón de células no pequeñas (CPCNP) escenificando utiliza el Clasificación de TNM. Esto se basa en el tamaño de la primaria tumor, ganglios linfáticos nparticipación de Oda y distante metastasis.[1]
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Utilizando los descriptores TNM, se asigna un grupo, que van desde cáncer oculto, a través de las etapas 0, IA (A uno), IB, IIA, IIB, IIIA, IIIB y IV (cuatro). Este grupo de etapa ayuda en la elección del tratamiento y la valoración del pronóstico.[65]
| TNM | Grupo de etapa |
|---|---|
| T1a-T1b N0 M0 | IA |
| T2a N0 M0 | IB |
| T1a, T2a N1 M0 | IIA |
| T2b N0 M0 | |
| T2b N1 M0 | IIB |
| T3 N0 M0 | |
| T1a-T3 N2 M0 | IIIA |
| T3 N1 M0 | |
| T4 N0, N1 M0 | |
| N3 M0 | IIIB |
| T4 N2 M0 | |
| M1 | IV |
Carcinoma de pulmón de células pequeñas (SCLC) tradicionalmente ha sido clasificado como "etapa limitada" (limitado a una mitad del pecho y en el ámbito de un solo tolerable radioterapia campo) o "etapa extensiva" (enfermedad más generalizada).[1] Sin embargo, la clasificación TNM y la agrupación son útiles en la estimación de pronóstico.[65]
Para CPNM y el SCLC, los dos tipos generales de escenificando las evaluaciones son estadiaje clínico y estadificación quirúrgica. Estadiaje clínico se realiza antes de la cirugía definitiva. Se basa en los resultados de estudios por imágenes (tales como Exploraciones del CT y Exploraciones del animal doméstico) y resultados de la biopsia. Estadificación quirúrgica se evalúa ya sea durante o después de la operación y se basa en los resultados combinados de resultados clínicos y quirúrgicos, incluyendo muestreo quirúrgico de los ganglios linfáticos torácicos.[8]
- Diagramas de características principales de la puesta en escena
-

Cáncer de pulmón de estadio IA y IB
-

Cáncer de pulmón en estadio IIA
-
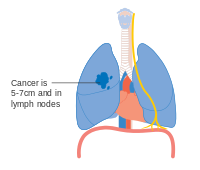
Cáncer de pulmón en estadio IIB
-

Una opción para la etapa de cáncer de pulmón IIB, con T2b; pero si el tumor es de 2 cm de la Carina, esto es etapa 3
-

Cáncer de pulmón estadio IIIA
-

Cáncer de pulmón estadio IIIA, si hay una característica de la lista a cada lado
-
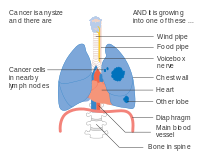
Cáncer de pulmón estadio IIIA
-

Cáncer de pulmón en estadio IIIB
-
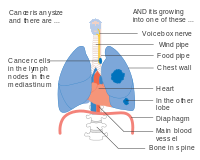
Cáncer de pulmón en estadio IIIB
-

Cáncer de pulmón estadio IV
Prevención
Prevención de fumar y dejar de fumar son formas eficaces de prevenir el desarrollo de cáncer de pulmón.[66]
Prohibición de fumar
Mientras que en la mayoría de los países han identificado carcinógenos industriales y domésticos y prohibido, fumar tabaco es aún generalizado. Eliminar el fumar de tabaco es un objetivo primordial en la prevención del cáncer de pulmón, y dejar de fumar es una herramienta preventiva importante en este proceso.[67]
Intervenciones de política para disminuir la tabaquismo pasivo en áreas públicas tales como restaurantes y lugares de trabajo se han convertido en más común en muchos países occidentales.[68] Bután ha tenido una prohibición completa de fumar desde 2005[69] mientras que la India introdujo la prohibición de fumar en público en octubre de 2008.[70] El Organización Mundial de la salud ha llamado a los gobiernos a una prohibición total de publicidad del tabaco para evitar que los jóvenes de que fumar. Evalúan que tales prohibiciones han reducido el consumo de tabaco por 16% donde instituyó.[71]
Proyección
Detección del cáncer utiliza exámenes médicos para detectar la enfermedad en grandes grupos de personas que no tienen síntomas.[72] Para los individuos con alto riesgo de desarrollar cáncer de pulmón, tomografía computada Proyección (TC) puede detectar el cáncer y dar a una persona opciones para responder a él de una manera que prolonga la vida.[57] Esta forma de cribado reduce la posibilidad de muerte por cáncer de pulmón por un valor absoluto de 0.3% (cantidad relativa del 20%).[73][74] Personas de alto riesgo son los 55-74 años que han fumado una cantidad equivalente de un paquete de cigarrillos diario durante 30 años como plazo los últimos 15 años.[57]
Proyección de CT se asocia con una alta tasa de falso positivo pruebas que pueden resultar en tratamiento innecesario.[75] Cada verdadero scan positivo hay unos 19 falsamente positivos escanea.[76] Otras preocupaciones incluyen exposición a la radiación[75] y el costo de las pruebas junto con seguimiento.[57] Investigación no ha encontrado dos otras pruebas disponibles,esputo citología de la o radiografía de tórax Pruebas de detección (CXR), para tener algún beneficio.[77]
El Tareas de servicios preventivos de Estados Unidos (USPSTF) recomienda el cribado anual mediante tomografía computarizada de dosis baja en aquellos que tienen una historia de fumar total de 30 años de pack y son entre 55 y 80 años hasta que una persona no ha estado fumando durante más de 15 años.[78] Proyección no se debe hacer en los otros salud problemas que tratamiento de cáncer de pulmón si encontraron no una opción.[78] El Inglés servicio nacional de salud fue en el 2014 vuelva a examinar la evidencia para la investigación.[79]
Otras estrategias de prevención
El uso prolongado de vitamina A suplementaria,[80][81] vitamina C,[80] la vitamina D[82] o vitamina E[80] no reduce el riesgo de cáncer de pulmón. Algunos estudios sugieren que las personas que consumen dietas con una mayor proporción de frutas y verduras tienden a tener un menor riesgo,[22][83] pero esto puede ser debido a factores de confusión— con el menor riesgo en realidad debido a la Asociación de una dieta alta frutas y verduras con menos fumadores. Estudios más rigurosos no han demostrado una asociación clara entre la dieta y del pulmón el riesgo de cáncer.[83]
Gestión
Tratamiento para el cáncer de pulmón depende del tipo de célula específica del cáncer, hasta qué punto ha propagacióny la persona Estado de rendimiento. Los tratamientos comunes incluyen cuidados paliativos,[84] cirugía, quimioterapia, y terapia de radiación.[1] Terapia dirigida del cáncer de pulmón está creciendo en importancia para el cáncer de pulmón avanzado.
Cirugía

Si las investigaciones confirman el NSCLC, el etapa se evalúa para determinar si la enfermedad está localizada y susceptibles de cirugía o si se ha propagado hasta el punto donde no se puede curar quirúrgicamente. Exploración por TAC y tomografía por emisión de positrones se utilizan para esta determinación.[1] Si se sospecha afectación ganglionar mediastínica, Mediastinoscopia puede utilizarse para muestra los nodos y ayudar a la puesta en escena.[85] Exámenes de sangre y pruebas de función pulmonar se utilizan para evaluar si una persona es lo suficientemente bien como para la cirugía.[14] Si las pruebas de función pulmonar revelan mala reserva respiratoria, cirugía no puede ser una posibilidad.[1]
En la mayoría de los casos de incipiente NSCLC, extirpación de un lóbulo del pulmón (lobectomía) es el tratamiento quirúrgico de elección. En pacientes no aptos para una lobectomía completo, un más pequeño (supresión sublobarresección en cuña) se puede realizar. Sin embargo, la resección de cuña tiene un riesgo mayor de recurrencia que la lobectomía.[86] Radiactivos yodo Braquiterapia al margen de la cuña la supresión puede reducir el riesgo de recurrencia.[87] En raras ocasiones, la extirpación de un pulmón entero (Neumonectomía) se lleva a cabo.[86] Cirugía thoracoscopic vídeo-asistida (IVAS) y VATS lobectomy Utilice un acercamiento como mínimo invasor para la cirugía de cáncer de pulmón.[88] VATS lobectomy es igualmente efectivo en comparación con lobectomía abierta convencional, con menos enfermedad postoperatoria.[89]
En SCLC, la quimioterapia o la radioterapia se utiliza normalmente.[90] Sin embargo, el papel de la cirugía en SCLC es ser reconsiderado. La cirugía podría mejorar los resultados cuando se añade a la quimioterapia y radiación en etapa temprana SCLC.[91]
Radioterapia
Radioterapia a menudo se administra junto con quimioterapia y puede utilizarse con intención curativa en pacientes con NSCLC que no son elegibles para la cirugía. Esta forma de radioterapia de alta intensidad se llama radioterapia radical.[92] Un refinamiento de esta técnica es la radioterapia hyperfractionated continua acelerada (carta), en que se administra una dosis alta de radioterapia en un corto período de tiempo.[93] Radioterapia torácica postoperatorio generalmente no puede usarse después de la cirugía de intención curativa para NSCLC.[94] Algunas personas con afectación de ganglionar mediastínica N2 pueden beneficiarse de radioterapia postoperatoria.[95]
Para los casos potencialmente curables en SCLC, radioterapia del tórax se recomienda además de la quimioterapia.[8]

Si una sección corta del bronquio, bloquea el crecimiento del cáncer Braquiterapia (radioterapia localizada) puede administrarse directamente dentro de la vía aérea para abrir el paso. En comparación con radioterapia externa, la braquiterapia permite una reducción en el tiempo de tratamiento y reduce la exposición del personal sanitario.[96] Pruebas para braquiterapia, sin embargo, son menor que para la radioterapia de haz externo.[97]
Irradiación craneal profiláctica (PCI) es un tipo de radioterapia en el cerebro, usado para reducir el riesgo de metástasis. PCI es más útil en SCLC. En la enfermedad de estadio, PCI aumenta tres años la supervivencia del 15% al 20%; en la enfermedad extensa, supervivencia de un año aumenta del 13% al 27%.[98]
Recientes mejoras en la orientación y proyección de imagen han llevado al desarrollo de la radiación estereotáctica en el tratamiento del cáncer de pulmón de la temprano-etapa. En esta forma de radioterapia, altas dosis se entregan sobre una serie de sesiones mediante técnicas de segmentación stereotactic. Su uso es principalmente en pacientes que no son candidatos a cirugía por médicos comorbilidades.[99]
Para pacientes con NSCLC y SCLC, pueden usarse dosis más pequeñas de radiación en el pecho para (control de síntomaspaliativos radioterapia).[100]
Quimioterapia
El quimioterapia régimen depende del tipo de tumor.[8] Carcinoma de pulmón de células pequeñas (SCLC), incluso relativamente temprana enfermedad, se trata principalmente con quimioterapia y radiación.[101] En SCLC, cisplatino y etopósido se utilizan más comúnmente.[102] Combinaciones con carboplatino, gemcitabina, paclitaxel, vinorelbina, topotecán, y irinotecan también se utilizan.[103][104] En el carcinoma pulmonar de células no pequeñas avanzado (CPCNP), la quimioterapia mejora la supervivencia y se utiliza como tratamiento de primera línea, siempre que la persona esté lo suficientemente bien como para el tratamiento.[105] Normalmente, se utilizan dos fármacos, de los cuales uno es a menudo basada en platino (ya sea cisplatino o carboplatino). Otros fármacos utilizados son gemcitabina, paclitaxel, docetaxel,[106][107] pemetrexed,[108] etopósido o vinorelbina.[107]
Quimioterapia adyuvante se refiere al uso de la quimioterapia después de cirugía aparentemente curativa para mejorar los resultados. En el CPCNP, se toman muestras de cerca los ganglios linfáticos durante la cirugía para ayudar a escenificando. Si se confirma la etapa II o III de la enfermedad, la quimioterapia adyuvante mejora la supervivencia en un 5% en cinco años.[109][110] La combinación de vinorelbina y cisplatino es más eficaz que los regímenes mayores.[110] Quimioterapia adyuvante para pacientes con Estadio IB del cáncer es polémica, como ensayos clínicos claramente no han demostrado un beneficio de supervivencia.[111][112] Quimioterapia antes de cirugía en el CPCNP que puede ser removido quirúrgicamente también parece mejorar los resultados.[113]
La quimioterapia puede combinarse con cuidados paliativos en el tratamiento del NSCLC. En casos avanzados, la quimioterapia apropiada mejora la promedio supervivencia sobre atención de apoyo sola, así como mejorar calidad de vida.[114] Con adecuada aptitud física mantenimiento de quimioterapia durante el tratamiento paliativo de cáncer de pulmón ofrece 1,5 a 3 meses de la prolongación de la supervivencia, alivio de los síntomas y una mejora en la calidad de vida, con mejores resultados consideradas los agentes modernos.[115][116] El grupo colaborativo de CPCNP metanálisis recomienda si el destinatario desea y puede tolerar el tratamiento, la quimioterapia debe considerarse en el CPCNP avanzado.[105][117]
Terapia dirigida
Varios fármacos que vías moleculares blanco en cáncer de pulmón están disponibles, especialmente para el tratamiento de la enfermedad avanzada. Erlotinib, Gefitinib y afatinib inhiben la cinasa de la tirosina en el receptor del factor de crecimiento epidérmico. Denosumab es un anticuerpo monoclonal dirigida contra receptor activador del ligando de factor nuclear kappa B. Puede ser útil en el tratamiento de las metástasis óseas.[118]
Cuidados paliativos
Cuidados paliativos Cuando se añade a atención oncológica habitual beneficia a gente incluso cuando todavía están recibiendo quimioterapia.[119] Estos enfoques permiten discusión adicional sobre opciones de tratamiento y proporcionan oportunidades para llegar a decisiones bien consideradas.[120][121] Cuidados paliativos pueden evitar el inútil pero costosa atención no sólo al final de la vida, pero también a través del curso de la enfermedad. Para las personas que han más avanzado la enfermedad, cuidado de hospicio también puede ser apropiado.[14][121]
Pronóstico
| Etapa clínica | Cinco años supervivencia (%) | |
|---|---|---|
| Carcinoma del pulmón de células no pequeñas | Carcinoma de pulmón de células pequeñas | |
| IA | 50 | 38 |
| IB | 47 | 21 |
| IIA | 36 | 38 |
| IIB | 26 | 18 |
| IIIA | 19 | 13 |
| IIIB | 7 | 9 |
| IV | 2 | 1 |
De las personas con cáncer de pulmón en los Estados Unidos, 16,8% sobrevive al menos cinco años después del diagnóstico.[10][122] En Inglaterra, entre 2005 y 2009, en general cinco años supervivencia para el cáncer de pulmón era menos del 10%.[123] Los resultados son generalmente peores en la mundo en desarrollo.[124] Etapa es avanzada a menudo en el momento del diagnóstico. En la presentación, son de 30-40% de los casos de CPCNP estadio IV, y 60% de SCLC son etapa IV.[8] Supervivencia para el cáncer de pulmón cae como la etapa en la diagnosis llega a ser más avanzada: el inglés datos sugieren que alrededor del 70% de los pacientes sobreviven por lo menos un año cuando se diagnostica en la etapa más temprana, pero esto cae a sólo 14% de aquellos diagnosticados con la enfermedad más avanzada.[125]
Factores pronósticos de CPNM incluyen la presencia o ausencia de síntomas pulmonares, tumor tamaño, tipo de celda)histología), grado de extensión (etapa) y metástasis a múltiples los ganglios linfáticos, y invasión vascular. Para las personas con enfermedad inoperable, los resultados son peores en los pobres Estado de rendimiento y pérdida de peso de más del 10%.[126] Factores pronósticos en cáncer de pulmón de células pequeñas incluyen estado de funcionamiento, Género, etapa de la enfermedad y la participación de la sistema nervioso central o hígado en el momento del diagnóstico.[127]
Para CPCNP, el mejor pronóstico se logra con resección quirúrgica completa de IA enfermedad, con hasta un 70% supervivencia a los cinco años.[128] Para SCLC, la supervivencia global de cinco años es alrededor del 5%.[1] Las personas con SCLC de etapa extensiva tienen una tasa promedio de cinco años de supervivencia de menos del 1%. El tiempo promedio de supervivencia para la enfermedad de estadio es 20 meses, con una tasa de supervivencia a cinco años del 20%.[2]
Según datos proporcionados por el Instituto Nacional del cáncer, la edad mediana en la diagnosis del cáncer de pulmón en los Estados Unidos es de 70 años,[129] y la edad promedio al morir es 72 años.[130] En los Estados Unidos, personas con seguro médico son más propensas a tener un mejor resultado.[131]
Epidemiología

|
no hay datos
≤ 5
5-10
10-15
15-20
20-25
25-30
|
30-35
35-40
40-45
45-50
50-55
≥ 55
|


En todo el mundo, el cáncer de pulmón es el cáncer más común entre los hombres en términos de ambos incidencia y mortalidad, y entre las mujeres tiene la tercera mayor incidencia y es el segundo después de cáncer de mama en la mortalidad. En 2012, hubo 1,82 millones de nuevos casos a nivel mundial y 1,56 millones de muertes debido a cáncer de pulmón, que representan el 19.4% de las muertes por cáncer.[11] Las tasas más altas son América del norte, Europa y Asia oriental, con más de un tercio de los nuevos casos en 2012 en China. Tarifas en África y Asia meridional son mucho más bajos.[133]
El segmento de población más propensos a desarrollar cáncer de pulmón es gente de edad más de 50 que tienen una historia de fumar. En contraste con la tasa de mortalidad en los hombres, que comenzó hace más de 20 años en declive, tasas de mortalidad de cáncer de pulmón de la mujer han ido en aumento durante las últimas décadas y recientemente están comenzando a estabilizar.[134] En los E.e.u.u., el riesgo de por vida del pulmón en desarrollo el cáncer es 8% en hombres y 6% en las mujeres.[1]
Por cada 3 millones cigarrillos fumó, uno se produce la muerte de cáncer de pulmón.[1][135] La influencia de"Big Tobacco"juega un papel importante en la cultura de fumar.[136] Jóvenes no fumadores que ven anuncios de tabaco son más propensos a tomar a fumar.[137] El papel de tabaquismo pasivo es cada vez más reconocida como un factor de riesgo para cáncer de pulmón,[25] hacia políticas de intervención para disminuir la exposición indeseada de los no fumadores a otros el humo del tabaco.[138] Las emisiones de los automóviles, fábricas y centrales eléctricas también plantean riesgos potenciales.[4]
Europa del este tiene la mayor mortalidad de cáncer de pulmón entre los hombres, mientras que el norte de Europa y Estados Unidos tienen la mortalidad más alta entre las mujeres. En los Estados Unidos, las mujeres y los hombres negros tienen una mayor incidencia.[139] Las tasas de cáncer de pulmón son actualmente inferiores en los países en desarrollo.[140] Con fumar creciente en los países en desarrollo, las tasas se esperan que aumente en los próximos años, especialmente en China[141] y la India.[142]
Cáncer de pulmón es el cáncer en segundo lugar más común en el Reino Unido (alrededor 43.500 personas fueron diagnosticadas con la enfermedad en 2011), y es la causa más común de muerte por cáncer (unos 35.400 personas murieron en el 2012).[143]
Desde la década de 1960, las tasas de adenocarcinoma de pulmón comenzaron a subir en relación con otros tipos de cáncer de pulmón. Esto es en parte debido a la introducción de cigarrillos de filtro. El uso de filtros elimina las partículas más grandes de humo de tabaco, lo que reduce la deposición en las vías respiratorias más grandes. Sin embargo, el fumador tiene que inhalar más profundamente para recibir la misma cantidad de nicotina, aumentando la deposición de partículas en las vías respiratorias pequeñas donde adenocarcinoma tiende a surgir.[144] La incidencia de adenocarcinoma de pulmón sigue aumentando.[145]
Historia
Cáncer de pulmón era poco común antes del advenimiento del tabaquismo; no fue incluso reconocido como una enfermedad distinta hasta 1761.[146] Diferentes aspectos del cáncer de pulmón fueron descritos más lejos en 1810.[147] Tumores malignos de pulmón compuestos solamente el 1% de todos los cánceres en la autopsia en 1878, pero se había levantado a 10 – 15% por el año 1900.[148] Informes del caso en la literatura médica numeran sólo 374 en todo el mundo en 1912,[149] pero una revisión de autopsias que la incidencia de cáncer de pulmón aumentaron de 0,3% en 1852 a 5.66% en 1952.[150] En Alemania en 1929, médico Fritz Lickint reconocido el vínculo entre fumar y cáncer de pulmón,[148] que condujo a una agresiva campaña antitabaco.[151] El Estudio de médicos británicos, publicado en la década de 1950, fue el primer sólido epidemiológica evidencia de la relación entre cáncer de pulmón y el tabaquismo.[152] Como resultado, en 1964 la Cirujano General de los Estados Unidos recomendado los fumadores deben dejar de fumar.[153]
La conexión con radón gas primero fue reconocido entre los mineros en la Montañas del mineral cerca de Schneeberg, Sajonia. Plata ha sido minado allí desde 1470 y estas minas son ricas en uranio, con el acompañamiento de su radio y gas radón.[154] Los mineros desarrollaron una cantidad desproporcionada de enfermedades pulmonares, finalmente reconocido como cáncer de pulmón en la década de 1870.[155] A pesar de este descubrimiento, explotación minera continuó en la década de 1950, debido a la URSSde demanda para el uranio.[154] Radón se confirmó como causa de cáncer de pulmón en la década de 1960.[156]
El primer éxito Neumonectomía de pulmón el cáncer fue realizado en 1933.[157] Paliativos radioterapia se ha utilizado desde la década de 1940.[158] Radioterapia radical, utilizada inicialmente en la década de 1950, fue un intento de utilizar grandes dosis de radiación en pacientes con cáncer de pulmón relativamente incipiente, pero que eran de otra manera impropios para la cirugía.[159] En 1997, acelerado continuo hyperfractionated la radioterapia fue vista como una mejora sobre la radioterapia radical convencional.[160] Pulmón de células pequeñas carcinoma inicial intentos en la década de 1960 en la resección quirúrgica[161] y radioterapia radical[162] fueron en vano. En la década de 1970, se desarrollaron los regímenes de quimioterapia exitosa.[163]
Direcciones de investigación
Direcciones de investigación actuales para el tratamiento de cáncer de pulmón incluyen inmunoterapia,[164] que estimula el sistema inmunológico para atacar las células del tumor, Epigenéticay nuevas combinaciones de quimioterapia y radioterapia, tanto por cuenta propia y juntos. Muchos de estos nuevos tratamientos trabajan a través de bloqueo de control inmune, alterar la capacidad del cáncer para evadir la sistema inmune.[164]
Ipilimumab bloques de señalización a través de un receptor de en Células T conocido como CTLA-4 que humedece el sistema inmune. Ha sido aprobado por la Administración de drogas y alimentos de Estados Unidos (FDA) para el tratamiento de melanoma y está experimentando ensayos clínicos para cáncer de pulmón de células no pequeñas (NSCLC) y cáncer de pulmón de células pequeñas (SCLC).[164]
Otros tratamientos de inmunoterapia interfieren con el atascamiento de muerte celular programada 1 Proteína (PD-1) con su ligand PD-1 ligando 1 (PD-L1). Señalización a través de PD-1 inactiva las células de T. Algunas células cancerosas parecen explotar esto expresando PD-L1 para activar las células T que pueden reconocer como una amenaza. Anticuerpos monoclonales dirigidos a PD-1 y PD-L1, tales como pembrolizumab y nivolumab[165] están actualmente en ensayos clínicos para el tratamiento de cáncer de pulmón.[164]
Epigenética es el estudio de pequeñas, generalmente hereditarias, molecular modificaciones – o 'clave' - que se unen a DNA y modificar expresión génica niveles. Dirigidos a estas 'etiquetas' con las drogas pueden matar las células cancerosas. Incipiente investigación en NSCLC con fármacos dirigidos a modificaciones epigenéticas muestra que el bloqueo a más de uno de estos 'tags' puede matar las células cancerosas con menos efectos secundarios.[166] Los estudios también demuestran que dar a los pacientes estas drogas antes de que el tratamiento estándar puede mejorar su eficacia. Ensayos clínicos están en curso para evaluar cómo estos medicamentos matan las células de cáncer de pulmón en los seres humanos.[166] Varios medicamentos dirigidos a mecanismos epigenéticos están en desarrollo. Inhibidores de histona deacetilasa en desarrollo incluyen ácido valproico, vorinostat, Belinostat, panobinostat, entinostat, y romidepsina. Metiltransferasa de ADN inhibidores en desarrollo incluyen decitabina, azacitidina, y Hidralazina.[52]
El proyecto TRACERx está buscando cómo CPCNP se desarrolla y evoluciona, y cómo estos tumores se vuelven resistentes al tratamiento.[167] El proyecto mira las muestras de tumor de 850 pacientes de CPCNP en diversas etapas, incluyendo diagnóstico, después del primer tratamiento, postratamiento y de la recaída.[168] Estudiar muestras en diferentes puntos del desarrollo del tumor, los investigadores esperan identificar los cambios impulsar el crecimiento tumoral y la resistencia al tratamiento. Los resultados de este proyecto ayudará a los científicos y los médicos obtener un mejor entendimiento de NSCLC y potencialmente conducen al desarrollo de nuevos tratamientos contra la enfermedad.[167]
Para los casos de cáncer de pulmón que desarrollan resistencia al receptor del factor de crecimiento epidérmico (EGFR) y quinasa del linfoma anaplástico de la (ALK) inhibidores de tirosina quinasa, medicamentos nuevos están en desarrollo. Nuevos inhibidores de EGFR incluyen afatinib y dacomitinib. Una vía alternativa de señalización, c-Met, puede ser inhibida por tivantinib y onartuzumab. Nuevos inhibidores de ALK incluyen Crizotinib y ceritinib.[169]
Referencias
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z Cuerno, L; PAO W; Johnson DH (2012). "Capítulo 89". En Longo, DL; Kasper, DL; Jameson, JL; Fauci, AS; Hauser, SL; Loscalzo, J. Principios de Harrison de medicina interna (18 ed). McGraw-Hill. ISBN 0-07-174889-X.
- ^ a b c "Carcinoma del pulmón: tumores de los pulmones". Merck Manual de edición profesional, edición en línea. 15 de agosto 2007.
- ^ Thun MJ, Hannan LM, Adams-Campbell LL, et al (septiembre de 2008). "ocurrencia de cáncer de pulmón en nunca-fumadores: un análisis de 13 cohortes y 22 estudios de registro de cáncer". PLoS Medicine 5 (9): e185. doi:10.1371/journal.pmed.0050185. PMC 2531137. PMID 18788891.
- ^ a b c d e f g h Alberg AJ, Samet JM (2010). "Capítulo 46". Murray & de Nadel libro de texto de medicina respiratoria (5ª ed.). Saunders Elsevier. ISBN 978-1-4160-4710-0.
- ^ a b O ' Reilly, KM; McLaughlin AM; Beckett WS; SIME PJ (marzo de 2007). "la enfermedad pulmonar relacionada con el asbesto". Médico de familia americano 75 (5): 683 – 688. PMID 17375514.
- ^ Carmona, RH (27 de junio de 2006). "consecuencias para la salud de la exposición involuntaria al humo de tabaco: un informe del Cirujano General". U.S. Departamento de salud y servicios humanos.
Exposición del humo de segunda mano causa enfermedad y muerte prematura en niños y adultos que no fuman.
Obtenido 2014-06-16 - ^ "El humo del tabaco y el fumar involuntario" (PDF). Monografías IARC en la evaluación de riesgos carcinógenos a los seres humanos (OMS International Agency for Research on Cancer) 83. 2004.
Hay suficiente evidencia que fumar involuntario (exposición al humo de tabaco de segunda mano o 'medio ambiente') provoca cáncer de pulmón en los seres humanos.... Fumadores involuntarios (exposición al humo de tabaco de segunda mano o 'medio ambiente') es carcinógeno para humanos (Grupo 1).
- ^ a b c d e f g h i j k Lu C, Onn A, Vaporciyan AA, et al (2010). «78: cáncer del pulmón ". Holland-Frei Cancer Medicine (8ª Ed.). Médica de la gente editorial. ISBN 978-1-60795-014-1.
- ^ Chapman, S; Robinson G; Stradling J; Oeste S (2009). «Capítulo 31». Manual Oxford de medicina respiratoria (2ª ed.). Prensa de la Universidad de Oxford. ISBN 978-0-19-954516-2.
- ^ a b "Programa de vigilancia, epidemiología y final resultados". Instituto Nacional del cáncer. 15 de julio 2014.
- ^ a b Informe sobre el cáncer Mundial 2014. Organización Mundial de la salud. 2014. pp. Capítulo 1.1. ISBN 9283204298.
- ^ Honnorat, J; Antoine JC (mayo de 2007). "Síndromes neurológicos Paraneoplásicos". Diario de Orphanet de enfermedades raras (BioMed Central) 2 (1): 22. doi:10.1186/1750-1172-2-22. PMC 1868710. PMID 17480225.
- ^ a b Greene, Frederick L. (2002). Manual puesta en escena de cáncer AJCC. Berlín: Springer-Verlag. ISBN 0-387-95271-3.
- ^ a b c d e Collins, LG; Haines C; Perkel R; Enck RE (enero de 2007). "cáncer de pulmón: diagnóstico y tratamiento". Médico de familia americano (Academia Americana de médicos de familia) 75 (1): 56 – 63. PMID 17225705.
- ^ Brown KM, Keats JJ, Sekulic A, et al (2010). "Capítulo 8". Holland-Frei Cancer Medicine (8ª Ed.). Médica de las personas publican los E.e.u.u. casa. ISBN 978-1-60795-014-1.
- ^ Biesalski HK, Bueno de Mesquita B, Chesson A, et al (1998). "Declaración de consenso europeo sobre el cáncer de pulmón: factores de riesgo y prevención. Panel de cáncer de pulmón". CA cáncer J Clin (Fumar es el factor de riesgo importante, representando cerca del 90% de incidencia de cáncer de pulmón). 48 (3): 167 – 176; discusión 164 – 166. doi:10.3322/canjclin.48.3.167. PMID 9594919.
- ^ a b Hecht, SS (2012). "Carcinogénesis de pulmón por el humo del tabaco". Diario internacional del cáncer de 131 (12): 2724-2732. doi:10.1002/IJC.27816. PMC 3479369. PMID 22945513.
- ^ Kumar, v.; Abbas AK; Aster JC (2013). "Capítulo 5". Patología básica de Robbins (9ª Ed.). Elsevier Saunders. p. 199. ISBN 978-1-4377-1781-5.
- ^ Peto R, Lopez AD, Boreham J, et al (2006). Mortalidad por tabaquismo en los países desarrollados 1950-2000: estimaciones indirectas de las estadísticas nacionales. Prensa de la Universidad de Oxford. ISBN 0-19-262535-7.
- ^ Agencia de protección ambiental de California (1997). "efectos en la salud de la exposición al humo ambiental del tabaco. Agencia de protección ambiental de California". Control del tabaco 6 (4): 346 – 353. doi:10.1136/TC.6.4.346. PMC 1759599. PMID 9583639.
- ^ Centers for Disease Control and Prevention (CDC) (Diciembre de 2001). "estado-prevalencia de tabaquismo actual entre los adultos y las políticas y actitudes sobre humo de segunda mano — Estados Unidos, 2000". Morbidity and Mortality Weekly Report (Atlanta, Georgia: CDC) 50 (49): 1101-1106. PMID 11794619.
- ^ a b c Alberg, AJ; Samet JM (septiembre de 2007). "Epidemiología del cáncer de pulmón". Pecho (Colegio Americano de Chest Physicians) 132 (S3): 29S-55S. doi:10.1378/Chest.07-1347. PMID 17873159.
- ^ Jaakkola, MS; Jaakkola JJ (agosto de 2006). "impacto de la legislación del lugar de trabajo libre de humo en exposiciones y salud: posibilidades de prevención". European Respiratory Journal 28 (2): 397-408. doi:10.1183/09031936.06.00001306. PMID 16880370.
- ^ Parkin, DM (diciembre de 2011). "tabaco, carga del cáncer atribuible en el Reino Unido en 2010". Diario británico del cáncer 105 (Suppl. 2): S6-S13. doi:10.1038/BJC.2011.475. PMC 3252064. PMID 22158323.
- ^ a b Taylor, R; Najafi F; Dobson (octubre de 2007). "meta-análisis de los estudios de tabaquismo pasivo y cáncer de pulmón: efectos del tipo de estudio y continente". Revista Internacional de Epidemiología 36 (5): 1048-1059. doi:10.1093/Ije/dym158. PMID 17690135.
- ^ «Preguntas frecuentes sobre humo de segunda mano». Organización Mundial de la salud. 25 de julio 2012.
- ^ Schick, S; Glantz S (diciembre de 2005). "experimentos toxicológicos de Philip Morris con dulce humo lateral: más tóxico que el humo de corriente principal". Control del tabaco 14 (6): 396 – 404. doi:10.1136/TC.2005.011288. PMC 1748121. PMID 16319363.
- ^ Greydanus, DE; Hawver EK; Greydanus MM (octubre de 2013). "marihuana: conceptos actuales". Fronteras en la salud pública 1 (42). doi:10.3389/fpubh.2013.00042. PMC 3859982. PMID 24350211.
- ^ Owen, KP; Sutter, ME; Albertson, TE (febrero de 2014). "marihuana: efectos de las vías respiratorias.". Comentarios clínicas en Alergia e Inmunología 46 (1): 65-81. doi:10.1007/s12016-013-8374-y. PMID 23715638.
- ^ Joshi, M; Joshi, A; Bartter, T (marzo de 2014). «marihuana y enfermedades pulmonares.». Opinión actual en medicina pulmonar 20 (2): 173-179. doi:10.1097/MCP.0000000000000026. PMID 24384575.
- ^ Tashkin, DP (junio de 2013). "Efectos de fumar marihuana en el pulmón". Anales de la sociedad torácica americana 10 (3): 239 – 47. doi:10.1513/annalsats.201212-127fr. PMID 23802821.
- ^ Underner, M; Urbano T; J Parriot (junio de 2014). "Cannabis tabaquismo y cáncer de pulmón". Des de la revista Maladies Respiratoires 31 (6): 488-498. doi:10.1016/j.RMR.2013.12.002. PMID 25012035.
- ^ Choi, H; Mazzone, P (septiembre de 2014). "radón y cáncer de pulmón: evaluar y mitigar el riesgo". Revista de clínica de Cleveland de la medicina 81 (9): 567-575. doi:10.3949/ccjm.81a.14046. PMID 25183848.
- ^ "Riesgos para la salud radón (Rn)". EPA.
- ^ K Schmid, Kuwert T, Drexler H (marzo de 2010). "radón en espacios interiores: un Factor de riesgo subestimado para el cáncer de pulmón en medicina ambiental". Dtsch Arztebl Int 107 (11): 181-6. doi:10.3238/Arztebl.2010.0181. PMC 2853156. PMID 20386676.
- ^ EPA (Febrero de 2013). "información de radiación: radón". EPA.
- ^ Tobias, J; Hochhauser D (2010). "Capítulo 12". Cáncer y su manejo (6ª Ed.). Wiley-Blackwell. p. 199. ISBN 978-1405-170154.
- ^ Davies, RJO; Lee YCG (2010). "18.19.3". Medicina libros de texto de Oxford (5ª ed.). Oxford University Press. ISBN 978-0-19-920485-4.
- ^ Chen, H; MS de Goldberg; Villeneuve PJ (Oct-Dic 2008). "Una revisión sistemática de la relación entre la exposición a largo plazo a la contaminación atmosférica y las enfermedades crónicas". Comentarios sobre salud ambiental 23 (4): 243 – 297. doi:10.1515/reveh.2008.23.4.243. PMID 19235364.
- ^ Clapp, RW; Jacobs MM; Loechler EL (Ene-Mar 2008). "causas ambientales y ocupacionales del cáncer de nueva evidencian, 2005 – 2007". Comentarios sobre salud ambiental 23 (1): 1 – 37. doi:10.1515/REVEH.2008.23.1.1. PMC 2791455. PMID 18557596.
- ^ a b Lim, Wyoming; Seow, (enero de 2012). "Biomasa combustibles y cáncer de pulmón.". Respirology (Carlton, Vic.) 17 (1): 20 – 31. doi:10.1111/j.1440-1843.2011.02088.x. PMID 22008241.
- ^ a b Sood, (diciembre de 2012). "exposición de combustible interior y el pulmón en el desarrollo de ambos países desarrollados: una actualización.". Clínicas en medicina de pecho 33 (4): 649 – 65. doi:10.1016/j.CCM.2012.08.003. PMID 23153607.
- ^ Yang, IA; Holloway, JW; Fong, KM (octubre de 2013). "Susceptibilidad genética al cáncer de pulmón y comorbilidades". Diario de la enfermedad torácica 5 (Suppl. 5): S454-S462. doi:10.3978/j.ISSN.2072-1439.2013.08.06. PMC 3804872. PMID 24163739.
- ^ Kern JA, McLennan G (2008). Enfermedades pulmonares y trastornos de Fishman (4ª Ed.). McGraw-Hill. p. 1802. ISBN 0-07-145739-9.
- ^ Larsen, JE; D de Minna (diciembre de 2011). "Biología Molecular del cáncer de pulmón: implicaciones clínicas". Clínicas en medicina de pecho 32 (4): 703 – 740. doi:10.1016/j.CCM.2011.08.003. PMC 3367865. PMID 22054881.
- ^ Cogliano, VJ; Baan, R; Straif, K; Grosse, Y; Lauby-Secretan, B; El Ghissassi, F; Bouvard, V; Benbrahim-Tallaa, L; Guha, N; Freeman, C; Galichet, L; Salvaje, CP (21 de diciembre de 2011). "Riesgos evitables asociados con cánceres humanos." (PDF). Revista del Instituto Nacional del cáncer 103 (24): 1827 – 39. doi:10.1093/jnci/djr483. PMID 22158127.
- ^ Cooper, WA; Lam el DLC; O ' Toole SA (octubre de 2013). "Biología Molecular del cáncer de pulmón" (PDF). Diario de la enfermedad torácica 5 (Suppl. 5): S. 479-490. doi:10.3978/j.ISSN.2072-1439.2013.08.03. PMC 3804875. PMID 24163741.
- ^ Tobias, J; Hochhauser D (2010). "Capítulo 12". Cáncer y su manejo (6ª Ed.). Wiley-Blackwell. p. 200. ISBN 978-1405-170154.
- ^ a b c d Herbst, RS; Heymach JV; Lippman SM (septiembre de 2008). "Cáncer de pulmón". Diario de Nueva Inglaterra de la medicina 359 (13): 1367-1380. doi:10.1056/NEJMra0802714. PMID 18815398.
- ^ Aviel-Ronen, S; Blackhall FH; Pastor FA; MS de Tsao (julio de 2006). "mutaciones de k-Ras en carcinoma del pulmón de la no-pequeño-célula: una revisión". Cáncer de pulmón clínico (Grupo de información de cáncer) 8 (1): 30 – 38. doi:10.3816/CLC.2006.n.030. PMID 16870043.
- ^ Kumar, v.; Abbas AK; Aster JC (2013). "Capítulo 5". Patología básica de Robbins (9ª Ed.). Elsevier Saunders. p. 212. ISBN 978-1-4377-1781-5.
- ^ a b Jakopovic, M; Thomas A; Balasubramaniam S (octubre de 2013). "contra el epigenoma en cáncer de pulmón: expansión de acercamientos a la terapia epigenética" (PDF). Fronteras en oncología 3 (261). doi:10.3389/FONC.2013.00261. PMC 3793201. PMID 24130964.
- ^ a b Mulvihill, MS; Kratz JR; Pham P (febrero de 2013). "el papel de las células madre en la reparación de la vía aérea: implicaciones para los orígenes del cáncer de pulmón". Diario chino de cáncer 32 (2): 71 – 74. doi:10.5732/CJC.012.10097. PMC 3845611. PMID 23114089.
- ^ Powell, CA; Halmos B; Nana – Sinkam SP (julio de 2013). "actualización en cáncer de pulmón y mesotelioma 2012" (PDF). Diario americano de la medicina respiratoria y crítica del cuidado 188 (2): 157-166. doi:10.1164/RCCM.201304-0716UP. PMC 3778761. PMID 23855692.
- ^ Miller, WT (2008). Enfermedades pulmonares y trastornos de Fishman (4ª Ed.). McGraw-Hill. p. 486. ISBN 0-07-145739-9.
- ^ Kaiser, LR (2008). Enfermedades pulmonares y trastornos de Fishman (4ª Ed.). McGraw-Hill. PP. 1815-1816. ISBN 0-07-145739-9.
- ^ a b c d e Médicos del Colegio Americano de pecho; American Thoracic Society (Septiembre de 2013), "cinco cosas que médicos y pacientes deben pregunta", Elegir sabiamente: una iniciativa de la Fundación ABIM (Los médicos del Colegio Americano de pecho y American Thoracic Society), obtenido 6 de enero 2013
- ^ a b Kumar, v.; Abbas AK; Aster JC (2013). "12". Patología básica de Robbins (9ª Ed.). Elsevier Saunders. p. 505. ISBN 978-1-4377-1781-5.
- ^ Subramanian, J; Govindan R (febrero de 2007). "cáncer de pulmón en no fumadores: una revisión". Revista de oncología clínica (Sociedad Americana de oncología clínica) 25 (5): 561-570. doi:10.1200/JCO.2006.06.8015. PMID 17290066.
- ^ Raz, DJ; Que B; R Rosell; Jablons DM (marzo de 2006). "carcinoma Bronchioloalveolar: una revisión". Cáncer de pulmón clínico 7 (5): 313 – 322. doi:10.3816/CLC.2006.n.012. PMID 16640802.
- ^ Rosti G, Bevilacqua G, Bidoli P, et al (marzo de 2006). "cáncer de pulmón de células pequeñas". Anales de la oncología 17 (Suppl. 2): 5 – 10. doi:10.1093/annonc/mdj910. PMID 16608983.
- ^ SEO JB, Im JG, Goo JM, et al (01 de marzo de 2001). "metástasis pulmonares atípicas: espectro de hallazgos radiológicos". Radiographics 21 (2): 403 – 417. doi:10.1148/Radiographics.21.2.g01mr17403. PMID 11259704.
- ^ D: tan Zander DS (2008). "inmunohistoquímica para la evaluación de neoplasias pulmonares y pleurales: una revisión y actualización". Int J Clin Exp Pathol 1 (1): 19 – 31. PMC 2480532. PMID ArgumentException: The incoming token has expired. Get a new access token from the Authorization Server. : ID=5641.V2_Json.Translate.1A5741B6.
- ^ Chheang, S; K marrón (junio de 2013). "estadificación del cáncer de pulmón: perspectivas clínicas y radiológicas". Seminarios en radiología intervencionista 30 (2): 99-113. doi:10.1055/s-0033-1342950. PMC 3709937. PMID 24436525.
- ^ a b c Rami-Porta, R; JJ de Crowley; Goldstraw P (febrero de 2009). "La TNM revisado escenificando sistema para cáncer de pulmón" (PDF). Anales de cirugía torácica y Cardiovascular 15 (1): 4 – 9. PMID 19262443.
- ^ Dela Cruz, CS; Tanoue LT; Volumen RA (diciembre de 2011). "cáncer de pulmón: Epidemiología, etiología y prevención" (PDF). Clínica de medicina de pecho 32 (4): 605 – 644. doi:10.1016/j.CCM.2011.09.001. PMC 3864624. PMID 22054876.
- ^ Goodman, GE (noviembre de 2002). "cáncer de pulmón. 1: prevención del cáncer de pulmón " (PDF). Tórax 57 (11): 994-999. doi:10.1136/Thorax.57.11.994. PMC 1746232. PMID 12403886.
- ^ McNabola, A; Gill LW (febrero de 2009). "el control de humo de tabaco ambiental: una revisión de la política". Revista Internacional de investigación ambiental y salud pública 6 (2): 741 – 758. doi:10.3390/ijerph6020741. PMC 2672352. PMID 19440413.
- ^ Pandey, G (febrero de 2005). "los fumadores de Bután enfrentan prohibición pública". BBC. 7 de septiembre 2007.
- ^ Pandey, G (02 de octubre de 2008). "India prohibición de fumar en público". BBC. 25 de abril 2012.
- ^ "Agencia de salud de la ONU pide prohibición total de publicidad del tabaco para proteger jóvenes" (Comunicado de prensa). Las Naciones Unidas Servicio de noticias. 30 de mayo de 2008.
- ^ Gutiérrez, A; R de SUH; F Abtin (junio de 2013). "Detección del cáncer de pulmón". Seminarios en radiología intervencionista 30 (2): 114 – 120. doi:10.1055/s-0033-1342951. PMC 3709936. PMID 24436526.
- ^ Jaklitsch MT, Jacobson FL, Austin JH, et al (julio de 2012). "La Asociación Americana para las pautas de la cirugía torácica para la detección del cáncer de pulmón con tomografía computarizada de dosis baja busca sobrevivientes de cáncer de pulmón y otros grupos de alto riesgo". Diario de cirugía torácica y Cardiovascular 144 (1): 33 – 38. doi:10.1016/j.jtcvs.2012.05.060. PMID 22710039.
- ^ De Bach PB, Mirkin JN, Oliver TK, et al (junio de 2012). "riesgos y beneficios del cribado de la CT para el cáncer de pulmón: una revisión sistemática". JAMA: el diario de la Asociación Médica Americana 307 (22): 2418-2429. doi:10.1001/Jama.2012.5521. PMC 3709596. PMID 22610500.
- ^ a b Aberle, D. R.; Abtin, f el.; Brown, K. (2013). ¿"computado tomografía cribado para el cáncer de pulmón: ha llegado finalmente? Implicaciones de la National Lung Screening Trial". Revista de oncología clínica 31 (8): 1002-1008. doi:10.1200/JCO.2012.43.3110. ISSN 0732-183 X.
- ^ De Bach PB, Mirkin JN, Oliver TK, et al (junio de 2012). "riesgos y beneficios del cribado de la CT para el cáncer de pulmón: una revisión sistemática". JAMA 307 (22): 2418-29. doi:10.1001/Jama.2012.5521. PMC 3709596. PMID 22610500.
- ^ Manser R, Lethaby A, Irving LB, C piedra, Byrnes G, Abramson MJ, Campbell D (2013). "Detección del cáncer de pulmón". Base de datos Cochrane de revisiones sistemáticas (6): CD001991. doi:10.1002/14651858.CD001991.pub3. PMID 23794187.
- ^ a b Moyer, VA; Tarea de servicios preventivos de Estados Unidos, fuerza (04 de marzo de 2014). "detección del cáncer de pulmón: Declaración de recomendación de la U.S. Preventive Services Task Force.". Anales de medicina interna 160 (5): 330 – 8. doi:10.7326/M13-2771. PMID 24378917.
- ^ Baldwin, DR; Hansell, DM; Duffy, SW; Campo, JK (07 de marzo de 2014). "cáncer de pulmón con dosis baja la tomografía computada.". BMJ (clínica investigación ed). 348: g1970. doi:10.1136/bmj.g1970. PMID 24609921.
- ^ a b c Fabricius, P; Lange P (julio – septiembre 2003). "dieta y cáncer de pulmón". Archivos de Monaldi de enfermedad torácica 59 (3): 207-211. PMID 15065316.
- ^ Fritz H, Kennedy D, Fergusson D, et al (2011). «Vitamina A y retinoides derivados de cáncer de pulmón: una revisión sistemática y Meta análisis». PLoS uno 6 (6): e21107. doi:10.1371/journal.pone.0021107. PMC 3124481. PMID 21738614.
- ^ Herr C, Greulich T, Koczulla RA, et al., (marzo de 2011). "el papel de la vitamina D en la enfermedad pulmonar: EPOC, asma, infección y cáncer". Investigación respiratoria 12 (1): 31. doi:10.1186/1465-9921-12-31. PMC 3071319. PMID 21418564.
- ^ a b Clave, TJ (enero de 2011). «riesgo de frutas y verduras y cáncer». Diario británico del cáncer 104 (1): 6 – 11. doi:10.1038/sj.BJC.6606032. PMC 3039795. PMID 21119663.
- ^ Ferrell, B; Koczywas M; Grannis F; Harrington (abril de 2011). "paliativos cuidados en cáncer de pulmón". Clínicas quirúrgicas de Norteamérica 91 (2): 403 – 417. doi:10.1016/j.Suc.2010.12.003. PMID 21419260.
- ^ Kaiser LR (2008). Enfermedades pulmonares y trastornos de Fishman (4ª Ed.). McGraw-Hill. PP. 1853-1854. ISBN 0-07-145739-9.
- ^ a b Kaiser LR (2008). Enfermedades pulmonares y trastornos de Fishman (4ª Ed.). McGraw-Hill. págs. 1855-1856. ISBN 0-07-145739-9.
- ^ Odell, DD; MS de Kent; Fernando HC (primavera de 2010). "resección sublobar con braquiterapia malla para etapa I cáncer de pulmón de células no pequeñas". Seminarios en cirugía torácica y Cardiovascular 22 (1): 32 – 37. doi:10.1053/j.semtcvs.2010.04.003. PMID 20813314.
- ^ Alam, N; Flores RM (julio – septiembre de 2007). "lobectomía cirugía torácica vídeo-asistida (IVAS): la base de pruebas". Revista de la sociedad de cirujanos de Laparoendoscopic 11 (3): 368-374. PMC 3015831. PMID 17931521.
- ^ Rueth, NM; Andrade RS (junio de 2010). "es mejor el lobectomy cubas: perioperatorio, biológicamente y oncologicamente?". Anales de cirugía torácica 89 (6): S2107-S2111. doi:10.1016/j.athoracsur.2010.03.020. PMID 20493991.
- ^ Simon GR, Turrisi (septiembre de 2007). "manejo del cáncer de pulmón de células pequeñas: guías de práctica clínica basada en evidencia de la ACCP (2ª edición)". Pecho 132 (3 Suppl): 324S-339S. doi:10.1378/Chest.07-1385. PMID 17873178.
- ^ Goldstein, SD; SC de Yang (octubre de 2011). "El papel de la cirugía en cáncer de pulmón de células pequeñas". Clínicas de cirugía oncológica de América del norte 20 (4): 769-777. doi:10.1016/j.soc.2011.08.001. PMID 21986271.
- ^ Arriagada, R; Goldstraw P; Le Chevalier T (2002). Libro de texto Oxford de Oncología (2ª ed.). Prensa de la Universidad de Oxford. p. 2094. ISBN 0-19-262926-3.
- ^ Hatton, MQ; JE de Martin (junio de 2010). "continua hiperfraccionada acelerada (carta) de la radioterapia y radioterapia no convencionalmente fraccionada en el tratamiento de cáncer de pulmón de células no pequeñas: una revisión y consideración de las direcciones futuras". Oncología Clínica (Colegio Real de radiólogos) 22 (5): 356-364. doi:10.1016/j.clon.2010.03.010. PMID 20399629.
- ^ Los autores del metanálisis puerto grupo (2005). Rydzewska, Larysa, ed. "Radioterapia postoperatoria para el cáncer de pulmón de células no pequeñas". Base de datos Cochrane de revisiones sistemáticas (2): CD002142. doi:10.1002/14651858.CD002142.pub2. PMID 15846628.
- ^ Le Péchoux, C (2011). "papel de la radioterapia postoperatoria en cáncer de pulmón de células no-pequeñas resecado: una nueva valoración basada en nuevos datos". Oncólogo 16 (5): 672-681. doi:10.1634/theoncologist.2010-0150. PMC 3228187. PMID 21378080.
- ^ Ikushima, H (febrero de 2010). "terapia de radiación: estado del arte y el futuro". Revista de investigación médica 57 (1-2): 1 – 11. doi:10.2152/JMI.57.1. PMID 20299738.
- ^ Reveiz, L; Rueda, JR; Cardona, AF (12 de diciembre de 2012). "la braquiterapia endobronquial paliativa para el cáncer de pulmón de células no pequeñas". La base de datos Cochrane de revisiones sistemáticas 12: CD004284. PMID 23235606.
- ^ Paumier, A; Cuenca X; Le Péchoux C (junio de 2011). "Irradiación craneal profiláctica en el cáncer de pulmón". Comentarios de tratamiento de cáncer 37 (4): 261-265. doi:10.1016/j.CTRV.2010.08.009. PMID 20934256.
- ^ Girard, N; F de Mornex (octubre de 2011). "la radioterapia de stereotactic para el cáncer de pulmón de células no pequeñas: del concepto a la realidad clínica. actualización 2011". Cáncer Radiothérapie 15 (6 – 7): 522-526. doi:10.1016/j.canrad.2011.07.241. PMID 21889901.
- ^ Fairchild A, Harris K, Barnes E, et al (agosto de 2008). "paliativa radioterapia torácica por cáncer de pulmón: una revisión sistemática". Revista de oncología clínica 26 (24): 4001-4011. doi:10.1200/JCO.2007.15.3312. PMID 18711191.
- ^ Hann CL, Rudin CM (30 de noviembre de 2008). "manejo del cáncer de pulmón de células pequeñas: cambios incrementales pero esperanza para el futuro". Oncología (Parque de Williston) 22 (13): 1486 – 92. PMID 19133604.
- ^ Murray, N; Turrisi (marzo 2006). "Una revisión del tratamiento de primera línea para el cáncer de pulmón de células pequeñas". Diario de la oncología torácica 1 (3): 270-278. PMID 17409868.
- ^ Azim, HA; Ganti AK (marzo de 2007). "Opciones de tratamiento para el cáncer de pulmón de células pequeñas recidivante". Medicamentos contra el cáncer 18 (3): 255 – 261. doi:10.1097/CAD.0b013e328011a547. PMID 17264756.
- ^ MacCallum, C; Gillenwater HH (julio de 2006). "tratamiento de segunda línea de cáncer de pulmón de células pequeñas". Informes actuales de la oncología 8 (4): 258 – 264. doi:10.1007/s11912-006-0030-8. PMID 17254525.
- ^ a b NSCLC metaanálisis Collaborative Group (octubre de 2008). "quimioterapia además de cuidados médicos de apoyo mejora la supervivencia en avanzado cáncer de pulmón de células no-pequeño: una revisión sistemática y metanálisis de datos de pacientes individuales de 16 ensayos controlados aleatorizaron". J. Clin. Oncol. 26 (28): 4617 – 25. doi:10.1200/JCO.2008.17.7162. PMC 2653127. PMID 18678835.
- ^ R de Mehra, tratar J (2008). Enfermedades pulmonares y trastornos de Fishman (4ª Ed.). McGraw-Hill. p. 1876. ISBN 0-07-145739-9.
- ^ a b Clegg A, Scott DA, Hewitson P, et al (enero de 2002). "eficacia clínica de paclitaxel, docetaxel, gemcitabina y vinorelbina en cáncer de pulmón de células no pequeñas: una revisión sistemática". Tórax (BMJ Publishing Group) 57 (1): 20 – 28. doi:10.1136/Thorax.57.1.20. PMC 1746188. PMID 11809985.
- ^ Fuld AD, Dragnev KH, Rigas JR (junio de 2010). "Pemetrexed en cáncer de pulmón de células no pequeñas avanzado". Expertos Opin Pharmacother 11 (8): 1387-402. doi:10.1517/14656566.2010.482560. PMID 20446853.
- ^ Carbone, DP; Felip E (septiembre de 2011). "terapia adyuvante en cáncer de pulmón de células no pequeñas: tratamiento futuras perspectivas y paradigmas". Cáncer de pulmón clínico 12 (5): 261 – 271. doi:10.1016/j.CLLC.2011.06.002. PMID 21831720.
- ^ a b Le Chevalier, T (octubre de 2010). "quimioterapia adyuvante para cáncer de pulmón de células no pequeñas resecable: donde va?". Anales de la oncología 21 (Suppl 7): vii196 – 198. doi:10.1093/annonc/mdq376. PMID 20943614.
- ^ Cuerno, L; Sandler AB; Putnam JB Jr; Johnson DH (mayo de 2007). "el fundamento de la quimioterapia adyuvante en etapa I el cáncer de pulmón de células no pequeñas". Diario de la oncología torácica 2 (5): 377 – 383. doi:10.1097/01.JTO.0000268669.64625.BB. PMID 17473651.
- ^ Wakelee, HA; Schiller JH; Dr. Gandara (julio de 2006). "estado actual de la quimioterapia adyuvante para el cáncer de pulmón de células no pequeñas IB etapa: implicaciones para el nuevo ensayo Intergroup". Cáncer de pulmón clínico (Grupo de información de cáncer) 8 (1): 18 – 21. doi:10.3816/CLC.2006.n.028. PMID 16870041.
- ^ NSCLC metanálisis colaborativo, grupo (03 de mayo de 2014). "la quimioterapia preoperatoria para el cáncer de pulmón de células no pequeñas: una revisión sistemática y metaanálisis de datos individuales de los participantes.". Lanceta 383 (9928): 1561 – 71. doi:10.1016/S0140-6736 (13) 62159-5. PMC 4022989. PMID 24576776.
- ^ Souquete PJ, Chauvin F, Boissel JP, Bernard JP (abril de 1995). "Meta-análisis de ensayos aleatorios de quimioterapia sistémica versus el tratamiento complementario en cáncer de pulmón de células no pequeñas no resecable". Cáncer de pulmón. 12 Suppl 1: S147 – 54. doi:10.1016/0169-5002 (95) 00430-9. PMID 7551923.
- ^ Sörenson S, Glimelius B, Nygren P (2001). "Una descripción sistemática de los efectos de la quimioterapia en cáncer de pulmón de células no pequeñas". Acta Oncologica 40 (2 – 3): 327 – 39. doi:10.1080/02841860151116402. PMID 11441939.
- ^ Clegg A Scott DA Sidhu M, Hewitson P, Waugh N (2001). "Una revisión rápida y sistemática de la efectividad clínica y costo-efectividad de paclitaxel, docetaxel, gemcitabina y vinorelbina en cáncer de pulmón de células no pequeñas". Evaluación de tecnologías de salud 5 (32): 1 – 195. PMID 12065068.
- ^ Cáncer de pulmón de células no pequeñas colaborativo, grupo (12 de mayo de 2010). "Quimioterapia y atención de apoyo versus atención de apoyo sola para el cáncer de pulmón de células no pequeñas avanzado". La base de datos Cochrane de revisiones sistemáticas (5): CD007309. doi:10.1002/14651858.CD007309.pub2. PMID 20464750.
- ^ D'Antonio; Passaro A; B de Gori (mayo de 2014). "cerebro y hueso metástasis en cáncer de pulmón: avances recientes en estrategias terapéuticas". Avances terapéuticos en oncología médica 6 (3): 101-114. doi:10.1177/1758834014521110. PMC 3987652. PMID 24790650.
- ^ Parikh, RB; Kirch, RA; Smith, TJ; TEMEL, JS (12 de diciembre de 2013). "Primera especialidad cuidados paliativos--traduciendo datos en oncología práctica.". El diario de Nueva Inglaterra de la medicina 369 (24): 2347 – 51. doi:10.1056/nejmsb1305469. PMC 3991113. PMID 24328469.
- ^ Según Kelley, DE Meier (agosto de 2010). "cuidados paliativos: un paradigma cambiante". Diario de Nueva Inglaterra de la medicina 363 (8): 781 – 2. doi:10.1056/NEJMe1004139. PMID 20818881.
- ^ a b Príncipe Paul M (abril de 2009). "cuando el Hospicio es la mejor opción: una oportunidad para redefinir los objetivos". Oncología (Parque de Williston, N.Y.) 23 (Ed de enfermera Suppl 4): 13 – 7. PMID 19856592.
- ^ Ridge, CA; McErlean AM; Ginsberg MS (junio de 2013). "Epidemiología del cáncer de pulmón". Seminarios en radiología intervencionista 30 (2): 93 – 98. doi:10.1055/s-0033-1342949. PMC 3709917. PMID 24436524.
- ^ "Estadísticas de supervivencia de cáncer de pulmón". Investigación de cáncer Reino Unido.
- ^ Majumder, editado por Sadhan (2009). Las células madre y cáncer (Online-Ausg. ed.). Nueva York: Springer. p. 193. ISBN 978-0-387-89611-3.
- ^ "Estadísticas de supervivencia de cáncer de pulmón". 28 de octubre 2014.
- ^ "Cáncer de pulmón de células no pequeñas tratamiento". PDQ para profesionales de la salud. Instituto Nacional del cáncer. 22 de noviembre 2008.
- ^ "Cáncer de pulmón de células pequeñas en tratamiento". PDQ para profesionales de la salud. Instituto Nacional del cáncer. 2012. 16 de mayo de 2012.
- ^ Spiro, SG (2010). "18.19.1". Medicina libros de texto de Oxford (5ª ed.). Oxford University Press. ISBN 978-0-19-920485-4.
- ^ Datos de la VIDENTE (del SEER.cancer.gov) Edad mediana de pacientes con cáncer en el diagnóstico 2002 – 2003
- ^ Datos de la VIDENTE (del SEER.cancer.gov) Edad mediana de pacientes con cáncer en muerte 2002 – 2006
- ^ Slatore, CG; Au DH; Gould MK (noviembre de 2010). "una revisión sistemática de la sociedad torácica americana oficial: estatus del seguro y las disparidades en los resultados y las prácticas de cáncer de pulmón". Diario americano de la medicina respiratoria y crítica del cuidado 182 (9): 1195-1205. doi:10.1164/RCCM.2009-038ST. PMID 21041563.
- ^ "país de lesiones y enfermedades de la OMS estima". Organización Mundial de la salud. 2009. 11 de noviembre 2009.
- ^ Stewart, editado por Bernard W.; Salvaje, Christopher P. (2014). Informe sobre el cáncer Mundial 2014. Lyon: Prensa IARC. págs. 350-352. ISBN 9789283204299.
- ^ Jemal A, Tiwari RC, Murray T, et al (2004). "Estadística del cáncer, 2004". CA: un diario del cáncer para los clínicos 54 (1): 8 – 29. doi:10.3322/canjclin.54.1.8. PMID 14974761.
- ^ Proctor, RN (marzo de 2012). "la historia del descubrimiento de la relación de cáncer pulmón cigarrillo: tradiciones probatorias, negación corporativo, peaje global". Control del tabaco 21 (2): 87 – 91. doi:10.1136/tobaccocontrol-2011-050338. PMID 22345227.
- ^ Lum, KL; Polansky JR; Jackler RK; Glantz SA (octubre de 2008). "firmado, sellado y entregado:"big tobacco» en Hollywood, 1927-1951". Control del tabaco 17 (5): 313-323. doi:10.1136/TC.2008.025445. PMC 2602591. PMID 18818225.
- ^ Lovato, C; Watts; Stead LF (octubre de 2011). "Impacto de la publicidad del tabaco y la promoción en el aumento de comportamientos de adolescentes fumadores". Base de datos Cochrane de revisiones sistemáticas (10): CD003439. doi:10.1002/14651858.CD003439.pub2. PMID 21975739.
- ^ Kemp, FB (Jul-Sep 2009). "humo libre las políticas en Europa. Un resumen". Pneumologia 58 (3): 155-158. PMID 19817310.
- ^ Instituto Nacional del cáncer; Hojas estadísticas VIDENTE: pulmón y bronquios. Vigilancia epidemiología y resultados finales. 2010 [1]
- ^ «Género en la investigación de fumar y cáncer de pulmón» (PDF). Organización Mundial de la salud. 2004. 26 de mayo 2007.
- ^ Zhang, J; Ou JX; Bai CX (noviembre de 2011). "fumar de tabaco en China: prevalencia, morbilidad, desafíos y estrategias de futuro". Respirology 16 (8): 1165-1172. doi:10.1111/j.1440-1843.2011.02062.x. PMID 21910781.
- ^ Behera, D; Balamugesh T (2004). "Cáncer de pulmón en la India" (PDF). Diario indio de enfermedades torácicas y ciencias afines 46 (4): 269-281. PMID 15515828.
- ^ "Estadísticas de cáncer de pulmón". Investigación de cáncer Reino Unido. 28 de octubre 2014.
- ^ Charloux A, Quoix E, Wolkove N, et al (febrero de 1997). ¿"la mayor incidencia de adenocarcinoma del pulmón: realidad o artefacto? Una revisión de la epidemiología de la adenocarcinoma del pulmón". Revista Internacional de Epidemiología 26 (1): 14 – 23. doi:10.1093/Ije/26.1.14. PMID 9126499.
- ^ Kadara, H; Kabbout M; Wistuba II (enero de 2012). "adenocarcinoma pulmonar: una entidad renovada en 2011". Respirology 17 (1): 50 – 65. doi:10.1111/j.1440-1843.2011.02095.x. PMID 22040022.
- ^ Morgagni, Giovanni Battista (1761). De sedibus et causis causis por anatomen indagatis. OL 24830495M.
- ^ Bayle, Gaspard-Laurent (1810). Recherches sur la phthisie pulmonaire (en francés). París. OL 15355651W.
- ^ a b Witschi, H (noviembre de 2001). "Una historia corta del cáncer de pulmón". Ciencias toxicológicas 64 (1): 4 – 6. doi:10.1093/toxsci/64.1.4. PMID 11606795.
- ^ Adler, I (1912). Crecimientos malos primarios de los pulmones y los bronquios. Nueva York: Longmans, Green, y Company. OCLC 14783544. OL 24396062M., citado en Spiro SG, Silvestri GA (2005). "cien años de cáncer de pulmón". Diario americano de la medicina respiratoria y crítica del cuidado 172 (5): 523 – 529. doi:10.1164/RCCM.200504-531OE. PMID 15961694.
- ^ Grannis, FW. "Historia del cigarrillo fumar y cáncer de pulmón". smokinglungs.com. archivado de la el original en 18 de julio de 2007. 6 de agosto 2007.
- ^ Proctor, R (2000). La guerra Nazi en cáncer. Prensa de la Universidad de Princeton. págs. 173-246. ISBN 0-691-00196-0.
- ^ Muñeca, R; Colina de AB (noviembre de 1956). "Cáncer de pulmón y otras causas de muerte en lo referente a fumar". British Medical Journal 2 (5001): 1071-1081. doi:10.1136/bmj.2.5001.1071. PMC 2035864. PMID 13364389.
- ^ Estados Unidos Departamento de salud educación y bienestar (1964). "tabaco y salud: informe de la Comisión Consultiva para el Cirujano General del servicio de salud pública" (PDF). Washington, DC: U.S. Goverment Printing Office.
- ^ a b Chicharrones, M (2000). Cáncer: el legado evolutivo. Prensa de la Universidad de Oxford. PP. 196 – 197. ISBN 0-19-262835-6.
- ^ Greenberg, M; Selikoff IJ (febrero de 1993). "cáncer de pulmón en las minas de Schneeberg: una reevaluación de los datos reportados por Harting y Hesse en 1879". Anales de la higiene en el trabajo 37 (1): 5 – 14. doi:10.1093/annhyg/37.1.5. PMID 8460878.
- ^ Samet, JM (abril de 2011). "riesgo de radiación y el cáncer: un continuo reto para los epidemiólogos". Salud ambiental 10 (Suppl. 1): S4. doi:10.1186/1476-069 X-10-S1-S4. PMC 3073196. PMID 21489214.
- ^ Cuerno, L; Johnson DH (julio de 2008). "Evarts A. Graham y la primera Neumonectomía por cáncer de pulmón". Revista de oncología clínica 26 (19): 3268-3275. doi:10.1200/JCO.2008.16.8260. PMID 18591561.
- ^ Edwards, en (1946). "Carcinoma bronquial". Tórax 1 (1): 1 – 25. doi:10.1136/THX.1.1.1. PMC 1018207. PMID 20986395.
- ^ Kabela, M (1956). «Erfahrungen mit der radikalen Röntgenbestrahlung des Bronchienkrebses» [experiencia con irradiación radical del cáncer bronquial]. Ceskoslovenská Onkológia (en alemán) 3 (2): 109-115. PMID 13383622.
- ^ Saunders M, Dische S, Barrett A, et al (julio de 1997). "continua hiperfraccionada acelerada (carta) de la radioterapia versus radioterapia convencional en el cáncer de pulmón de células no pequeñas: un ensayo de multicéntricos aleatorios". Lanceta (Elsevier) 350 (9072): 161-165. doi:10.1016/S0140-6736 (97) 06305-8. PMID 9250182.
- ^ Lennox SC, Flavell G, Pollock DJ, et al., (noviembre de 1968). «Resultados de la resección del carcinoma de células de avena del pulmón». Lanceta (Elsevier) 2 (7575): 925-927. doi:10.1016/S0140-6736 (68) X 91163. PMID 4176258.
- ^ Miller, AB; Fox W; R alto (septiembre de 1969). "seguimiento de cinco años del ensayo comparativo Consejo de investigación médica de la cirugía y la radioterapia para el tratamiento primario del carcinoma pequeño-celled o avena-celled del bronquio". Lanceta (Elsevier) 2 (7619): 501-505. doi:10.1016/S0140-6736 (69) 90212-8. PMID 4184834.
- ^ Creaven PJ, Cohen M, Fossieck ser Jr et al (1977). "Quimioterapia intensiva de carcinoma broncogénico de células pequeñas". Informes del tratamiento de cáncer 61 (3): 349-354. PMID 194691.
- ^ a b c d Brahmer, JR. (febrero de 2014). "bloqueo de control inmune: la esperanza de la inmunoterapia como tratamiento del cáncer de pulmón?". Seminarios en oncología 41 (1): 126-32. doi:10.1053/j.seminoncol.2013.12.014. PMID 24565586.
- ^ Powell, CA; Halmos, B; Nana-Sinkam, SP (julio de 2013). "actualización en cáncer de pulmón y mesotelioma 2012". Diario americano de la medicina respiratoria y crítica del cuidado 188 (2): 157-166. doi:10.1164/RCCM.201304-0716UP. PMC 3778761. PMID 23855692.
- ^ a b Forde, PM; Brahmer, JR; Kelly, RJ (01 de mayo de 2014). "nuevas estrategias en cáncer de pulmón: terapia Epigenética para cáncer de pulmón de células no pequeñas.". Investigación de cáncer clínica: un diario oficial de la American Association for Cancer Research 20 (9): 2244-8. doi:10.1158/1078-0432.CCR-13-2088. PMID 24644000.
- ^ a b Jamal-Hanjani, M; Hackshaw, A; Ngai, Y; et al (julio de 2014). "seguimiento evolución genómica del cáncer medicina de precisión: el estudio TRACERx del pulmón.". Biología de PLOS 12 (7): e1001906. doi:10.1371/journal.pbio.1001906. PMID 25003521.
- ^ Proyecto de TRACERx, blog de ciencia de la investigación de cáncer Reino Unido
- ^ Spaans, JN. Goss, GD (agosto de 2014). "ensayos para vencer la resistencia de la droga a EGFR y ALK dirigido terapias — pasado, presente y futuro". Fronteras en oncología 4 (233). doi:10.3389/FONC.2014.00233. PMC 4145253. PMID 25221748.
Acoplamientos externos
| Campos comunes de Wikimedia tiene medios relacionados con Cánceres de pulmón. |
- Cáncer de pulmón en DMOZ
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Otras Páginas
- Incidentes en Walt Disney World
- Comite Nacional de facturacion uniforme
- Sukhothai Thammathirat Open University
- Prestamos de asistencia de marketing
- GA 2011
- Jack Thompson (activista) (redireccion de Jack Thompson (abogado))
- Relacion prestamo a valor
- Blackphone
- Johannes Dinkwanyane
- Cromatina sal y pimienta
- Motor de combustion externa
- Lista de los psicologos positivos
- Almacen de datos
- Lanzador X
- George Calvert, 1r baron Baltimore









