Inactivación de X


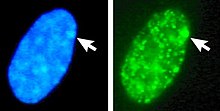
Izquierda: ADN (DAPI)-tinción de núcleo. La flecha indica la ubicación de body(Xi) Barr. Derecha: ADN asociado histonas detectadas la proteína
Inactivación de X (también llamado lyonization) es un proceso por el cual una de las dos copias de la Cromosoma x presente en mujer mamíferos es inactivado. El cromosoma de X inactivo es silenciado por sus empaquetados de tal manera que tiene una estructura transcripcionalmente inactiva llamada heterocromatina. Como casi todos los hembra mamíferos tienen dos cromosomas X, X-inactivación les impide tener doble cromosoma X productos del gen como machos, que sólo poseen una sola copia del cromosoma X (véase compensación de dosis). La elección de que se hecho inactivo cromosoma X es aleatoria en mamíferos placentarios tales como seres humanos, pero una vez que un cromosoma X es inactivado permanecerá inactivo durante toda la vida de la célula y sus descendientes en el organismo. A diferencia de la aleatoria inactivación X en mamíferos placentarios, la inactivación de marsupiales se aplica exclusivamente al cromosoma de X paternal derivado.
Contenido
- 1 Historia
- 2 Mecanismo de
- 2.1 Tiempo
- 2.2 Selección de un cromosoma X activo
- 2.3 Componente cromosómico
- 2.4 Xist y Tsix RNAs
- 2.5 Silenciamiento
- 2.6 Cuerpos de Barr
- 2.6.1 Genes expresados en el cromosoma de X inactivo
- 3 Usos en biología experimental
- 4 Véase también
- 5 Referencias
- 6 Lectura adicional
Historia
En 1959 Susumu Ohno demostró que los dos X-cromosomas de mamíferos eran diferentes: uno parecía similar a la autosomas; el otro era condensada y heterochromatic.[3] Este hallazgo sugiere, independientemente para dos grupos de investigadores, que uno de los X-cromosomas experimentó la inactivación. En 1961, Mary Lyon propuesto la inactivación al azar de un cromosoma X femenino para explicar el fenotipo moteado de ratones femeninos heterozigótica para el color de la capa genes.[4] La hipótesis de Lyon también representan los resultados que una copia del cromosoma X en las células femeninas fue altamente condensada, y que ratones con solamente una copia del cromosoma X desarrollaron como hembras infértiles. Esto sugiere[5] Para Ernest Beutler, estudiando las hembras heterozigóticas para Glucosa-6-fosfato deshidrogenasa Deficiencia de (G6PD), que había dos poblaciones de glóbulos rojos de los eritrocitos en estos heterocigotos: células deficientes y las células normales,[6] dependiendo de si el cromosoma X inactivado contiene el alelo normal o defectuoso de la G6PD.
Mecanismo de
Tiempo
Todas las células de ratón se someten a una temprana impreso inactivación del cromosoma de X paternal derivado en etapa de dos células o cuatro células embriones.[7][8][9] El extraembrionarias tejidos (que dan lugar a la placenta y otros tejidos apoyando el embrión) retener esta inactivación impresa temprana, y así sólo el cromosoma de X maternal activo en estos tejidos.
En los primeros blastocisto, esta inactivación de X inicial, impresa está invertida en las células de la masa celular interna (que dan lugar al embrión), y en estas células ambos cromosomas de X activos otra vez. Cada una de estas células después de forma independiente y al azar inactiva una copia del cromosoma X.[9] Este evento de la inactivación es irreversible durante la vida de la célula, por lo que todos los descendientes de una célula que inactivo un cromosoma particular inactivan también ese mismo cromosoma. Este fenómeno, que se observan en la coloración del gatos Carey Cuando las hembras son heterozigótica para la Gene X-ligado, no se debe confundir con mosaicism, que es un término que se refiere específicamente a las diferencias en la genotipo de distintas poblaciones celulares en el mismo individuo; X-inactivación, que es un epigenéticos cambio que resulta en un fenotipo diferente, es no un cambio en la genotípico nivel. Para una célula individual o un linaje la inactivación es por lo tanto sesgada o 'no aleatoria', y esto puede dar lugar a síntomas leves en mujeres portadoras de X-ligado trastornos genéticos.[10]
Inactivación de X se invierte en la mujer línea germinal, para que todos ovocitos contienen un cromosoma de X activo.
Selección de un cromosoma X activo
Las hembras normales poseen dos cromosomas, X y en cualquier célula dada un cromosoma será activo (señalado como Xa) y uno inactivo (Xi). Sin embargo, los estudios de individuos con copias adicionales del cromosoma X muestran que en las células con más de dos cromosomas X es Xa sólo uno y los restantes cromosomas X están inactivados. Esto indica que el estado por defecto del cromosoma X en las hembras es la inactivación, pero un cromosoma de X es siempre seleccionado para permanecer activo.
Se entiende que la inactivación del X-cromosoma es un proceso aleatorio, que ocurren en el tiempo de Gastrulation En epiblasto (las células que darán lugar al embrión). Maternal y paternal cromosomas X tienen una igual probabilidad de inactivación. Esto sugeriría que las mujeres, se estima que sufren de desórdenes X-ligados aproximadamente el 50% tan a menudo como los hombres[citación necesitada] (porque las mujeres tienen dos cromosomas, X mientras que los hombres tienen sólo uno); sin embargo, en realidad, es mucho más baja que la aparición de estos trastornos en las mujeres. Una explicación para esta disparidad es que más del 25% de los genes en el cromosoma X inactivado siguen siendo expresadas, proporcionando a las mujeres protección añadida contra genes defectuosos codificadas por el cromosoma x. Algunos[¿quién?] sugieren que esta disparidad debe ser prueba de inactivación (no aleatoria) preferencial. Inactivación preferencial del cromosoma paterno se produce en dos marsupiales y en linajes de células que forman las membranas que rodean el embrión,[11] pero no ocurre en la mayoría de nuestras células[citación necesitada].
El plazo para la inactivación del X-cromosoma, explica esta disparidad. La inactivación ocurre en el epiblasto durante la gastrulación, que da lugar al embrión.[12] La inactivación se produce a nivel celular, resultando en una expresión de mosaico, en que parches de células con un cromosoma de x maternal inactivo, mientras que los otros parches tienen un cromosoma de x paternal inactivo. Por ejemplo, una hembra heterozigótica de hemofilia (una enfermedad x-ligada) tendría alrededor de la mitad de sus células del hígado funcionando correctamente, que suele ser suficiente para asegurar la normal coagulación de la sangre.[13][14] Posibilidad de causar células significativamente más disfuncionales; sin embargo, están poco probable que tales extremos estadísticos. Diferencias genéticas en el cromosoma también pueden representar un X-cromosoma más propensos a sufrir inactivación. También, si un cromosoma tiene una mutación que obstaculizan su crecimiento o que lo hacen no viable, las células que se inactiva al azar que X tendrá una ventaja selectiva sobre las células que se inactiva al azar el alelo normal. Así, aunque la inactivación es al azar inicialmente, células que inactivan un alelo normal (dejando el alelo mutado activo) serán finalmente invadidas y sustituidas por células funcionalmente normales en que casi todos tienen el mismo cromosoma x activado.[13]
Se presume[¿por quién?] existe un autosomally codificado 'bloqueo factor' que se une al cromosoma X y evita su inactivación. El modelo postula que existe una limitante de bloqueo, por lo que una vez que la molécula de factor de bloqueo disponibles une a un cromosoma de X el resto de X chromosome(s) no están protegidos de inactivación. Este modelo es apoyado por la existencia de un solo Xa en células con cromosomas X muchos y por la existencia de dos cromosomas en las líneas celulares con el doble del número normal de autosomas X activo.[15]
Secuencias en la Centro de inactivación del X (XIC), presente en el cromosoma X, control de silenciamiento del cromosoma X. El hipotético factor de bloqueo se prevé que se unen a secuencias en el XIC.
Componente cromosómico
|
|
En esta sección no citar cualquier fuentes. (Octubre de 2014) |
El centro de inactivación de X (o simplemente XIC) en el cromosoma X es necesarias y suficientes provocar la inactivación de X. Translocaciones cromosómicas que coloque el XIC en un autosome conduzca a inactivación de la autosome, y cromosomas X que carecen el XIC no se inactivan.
El XIC contiene cuatro no-Texto traducido al RNA genes, XIst, Tsix, HP: y FTX, que están implicadas en la inactivación de X. El XIC también contiene sitios de Unión para conocidos y desconocidos proteínas reguladoras.
Xist y Tsix RNAs
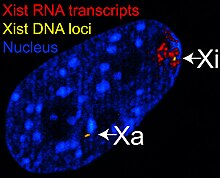
El X inactivo (de transcripción específicosXIst) el gene codifica un grande RNA no codificante es responsable de mediar el silenciamiento específico del cromosoma X que se transcribe.[16] El cromosoma de X inactivo es cubierto por el RNA de Xist,[17] mientras que el Xa no es (ver figura a la derecha). El gene de Xist es el único gene que es expresado desde el Xi, pero no de la Xa. Cromosomas X que carecen el gene de Xist no pueden ser inactivados.[18] Colocando artificialmente y expresando el gen Xist en otro cromosoma conduce a silenciar ese cromosoma.[19][20]
Antes de la inactivación, ambos cromosomas débil X expresan Xist RNA del gen Xist. Durante el proceso de inactivación, el futuro Xa deja expresar Xist, mientras que el Xi futuro aumenta dramáticamente la producción de RNA de Xist. En el Xi futuro, el RNA de Xist cubre progresivamente el cromosoma, que se extiende hacia fuera desde el XIC;[19] el RNA de Xist no localizar a la Xa. El silenciamiento de genes a lo largo del Xi se produce poco después de la capa por el RNA de Xist.
Como Xist, el Tsix gen codifica un RNA grande que no se cree que codifican una proteína. Se transcribe el RNA de Tsix antisentido a Xist, significando que el gene de Tsix traslapa el gene de Xist y es transcripción en el filamento opuesto de DNA desde el gen Xist.[21] Tsix es un regulador negativo de Xist; Cromosomas x que carecen la expresión de Tsix (y así tener altos niveles de Xist transcripción) se inactivan mucho más con frecuencia que los cromosomas normales.
Como Xist, antes de la inactivación, ambos cromosomas débil X expresan RNA de Tsix desde el gene de Tsix. Sobre el inicio de la inactivación de X, el Xi futuro deja de expresar el RNA de Tsix (y aumenta la expresión de Xist), mientras que Xa continúa express Tsix durante varios días.
Silenciamiento
El cromosoma de X inactivo no expresa la mayoría de sus genes, a diferencia del cromosoma de X activo. Esto es debido al silenciamiento de la Xi por represivo heterocromatina, que compacta el ADN Xi y previene la expresión de la mayoría de los genes.
En comparación con el Xa, Xi tiene altos niveles de Metilación del ADN, bajos niveles de acetilación de histonas, bajos niveles de histona H3 lisina-4 metilacióny niveles altos de metilación de la lisina 9 de la histona H3, todos los cuales están asociados con silenciamiento génico.[22] Además, una variante de la histona llamada macroH2A (H2AFY) se encuentra exclusivamente en nucleosomas a lo largo de Xi.[23][24]
Cuerpos de Barr
ADN en la heterocromatina, como la Xi, es más condensada de ADN empaquetado en eucromatina, como la Xa. El X inactivo forma un cuerpo discreto dentro del núcleo denominado un Cuerpo de Barr.[25] El cuerpo de Barr se encuentra generalmente en la periferia de la núcleo, es tarde replicación de dentro de la ciclo celulary, como contiene el Xi, contiene modificaciones de heterocromatina y el RNA de Xist.
Genes expresados en el cromosoma de X inactivo
Escapar de una fracción de los genes en el cromosoma X inactivación en el Xi. El gene de Xist es expresado en altos niveles en el Xi y no se expresa en la Xa.[26] Muchos otros genes escapan de inactivación; algunos se expresan igualmente de la Xa y Xi, y otros, expresó de ambos cromosomas, aún predominante se expresan de la Xa.[27][28][29] Hasta una cuarta parte de los genes en el Xi humano son capaces de escapar.[27] Estudios en el ratón sugieren que en cualquier tipo celular dado, 3% a 15% de los genes escapar de inactivación, y que escapar identidad gen varía entre los tejidos.[28][29]
Muchos de los genes que inactivación de escape están presentes a lo largo de las regiones del cromosoma X que, a diferencia de la mayoría del cromosoma X contienen genes presentan también en la Cromosoma de y. Estas regiones se denominan pseudoautosomal regiones, como individuos de uno u otro sexo recibirán dos copias de cada gen en estas regiones (como un autosome), desemejante de la mayoría de los genes a lo largo de los cromosomas sexuales. Puesto que las personas de cualquier sexo recibirán dos copias de cada gen en un región pseudoautosomal, ninguna compensación de dosis es necesaria para las mujeres, por lo que se postula que estas regiones de ADN han evolucionado mecanismos para escapar x-inactivación. Los genes de las regiones pseudoautosomal del Xi no tienen las típicas modificaciones de la Xi y poco RNA de Xist limitado.
La existencia de los genes a lo largo del X inactivo que no se calla explica los defectos de los seres humanos con números anormales del cromosoma X, tales como Síndrome de Turner (X 0) o Síndrome de Klinefelter (XXY). Teóricamente, la x-inactivación debe eliminar las diferencias en la dosificación del gene entre los individuos afectados e individuos con una dotación de cromosomas normal. En los individuos afectados, sin embargo, x-inactivación es incompleta y la dosificación de estos genes silenciados no será diferente como se escapa x-inactivación, similar a una aneuploidía autosómica.
Los mecanismos precisos que escape control de inactivación de X no se conocen, pero silenciado y escapar de las regiones han demostrado tener marcas distintas de la cromatina.[28][30] Se ha sugerido que escape de la x-inactivación podría estar mediado por la expresión de largo no codificante del RNA (lncRNA) dentro de los dominios cromosómicos escapando.[2]
Usos en biología experimental
Stanley Michael Gartler utiliza inactivación cromosoma X para demostrar el origen clonal de los cánceres. Examen de los tejidos normales y tumores de las hembras heterozigóticas para isoenzimas de la ligada al sexo G6PD gene demostraron que las células del tumor de tales individuos expresan sólo una forma de G6PD, mientras que los tejidos normales se componen de una mezcla casi igual de las células que expresan los dos fenotipos diferentes. Este patrón sugiere que una sola célula y no una población, crece en un cáncer.[31] Sin embargo, este patrón ha demostrado incorrecto para muchos tipos de cáncer, sugiriendo que algunos tipos de cáncer pueden ser de origen policlonales.[32]
Además, de medir el estado de metilación (inactivación) del receptor de andrógenos humano polimórfico (HUMARA) localizado en el cromosoma x se considera el método más preciso para evaluar la clonalidad en biopsias de cáncer femenino.[33] Una gran variedad de tumores fue probada por este método, algunos, como el carcinoma de células renales,[34] encuentra monoclonal mientras que otros (por ejemplo, mesotelioma[35]) se reportaron policlonal.
Los investigadores también han estudiado mediante la inactivación del X-cromosoma para silenciar la actividad de cromosomas autosómicos. Por ejemplo, Jiang et al. inserta una copia del gen Xist en una copia del cromosoma 21 en células madre derivado de una persona con trisomía 21 (Síndrome de Down).[36] El gene de Xist insertado induce la formación del cuerpo de Barr, desencadena modificaciones estable de la heterocromatina y silencia la mayor parte de los genes en la copia extra del cromosoma 21. En estas células madre modificadas, el silenciamiento génico mediado Xist parece revertir algunos de los defectos asociados con síndrome de Down.
Véase también
- Sistema de determinación del sexo
- Compensación de dosis
- Cuerpo de Barr
- Heterocromatina
- Epigenética
- X-inactivación sesgada
- Trastornos del desarrollo parece estar relacionado con la inactivación de X:
- Encefalopatía epiléptica, temprana infantil, 9
- Displasia de frontonasal
Referencias
- ^ Gartler SM, Varadarajan KR, Luo P, Canfield TK, Traynor J, Francke U, Hansen RS (2004). "modificaciones de las histonas normal en el cromosoma de X inactivo en las células de síndrome ICF y Rett: implicaciones para el metil- / 2/21/Figura/F1 Figura 1".
- ^ a b Björn Reinius, Chengxi Shi, Liu Hengshuo, Kuljeet Singh Sandhu, Katarzyna J. Radomska, Glenn D. Rosen, Lu Lu, Klas Kullander, Robert w. Williams y Elena Jazin (noviembre de 2010). «Mujer parcial expresión de ARN largo no codificante en ámbitos que escapan a la inactivación de X en ratón». BMC Genomics 11: 614. doi:10.1186/1471-2164-11-614. PMC3091755. PMID21047393.
- ^ Ohno S, Kaplan WD, Kinosita R (1959). "Formación de la cromatina sexual por un solo cromosoma x en las células del hígado de rattus norvegicus". Res de exp de la célula 18 (2): 415 – 9. doi:10.1016/0014-4827 (59) 90031-X. PMID14428474.
- ^ MF de Lyon (1961). "acción génica en la X-cromosoma del ratón (Mus musculus L.)". Naturaleza (Resumen) 190 (4773): 372 – 3. doi:10.1038/190372a0. PMID13764598.
- ^ Beutler, E (enero de 2008). "deficiencia de deshidrogenasa de glucosa-6-fosfato: una perspectiva histórica". Sangre 111 (1): 16 – 24. doi:10.1182/sangre-2007-04-077412. PMID18156501.
- ^ Beutler E, Yeh M, Fairbanks VF (enero de 1962). "LA HEMBRA HUMANA NORMAL COMO UN MOSAICO DE ACTIVIDAD DEL CROMOSOMA X: ESTUDIOS USANDO EL GENE FOR G-6-PD-DEFICIENCIA COMO UN MARCADOR". Estados Unidos el proc. nacional Acad. SCI. 48 (1): 9 – 16. doi:10.1073/pnas.48.1.9. PMC285481. PMID13868717.
- ^ Takagi N, Sasaki M (1975). "Inactivación preferencial del cromosoma de X paternal derivado en las membranas extraembrionarias del ratón". Naturaleza 256 (5519): 640-2. doi:10.1038/256640a0. PMID1152998.
- ^ Cheng MK, Disteche CM (2004). "silencio de los padres: primeros X inactivación". Diseñó 26 (8): 821-4. doi:10.1002/bies.20082. PMID15273983.
- ^ a b Okamoto, Otte A, Allis C, D de Reinberg, escuché E (2004). "epigenética dinámica de impreso X inactivación durante el desarrollo temprano del ratón". Ciencia 303 (5658): 644-9. doi:10.1126/Science.1092727. PMID14671313.
- ^ Puck, J; Willard, HF (1998). "X inactivación en las mujeres con enfermedades ligadas al cromosoma X". N. Engl. J. Med. 338 (5): 325-8. doi:10.1056/NEJM199801293380611. PMID9445416.
- ^ Sepulcros de JAM (1996). "animales que rompen las reglas: genética de marsupiales y monotremas". Revisión anual de la genética. www.annualreviews.org: Nature Publishing Group. PP. 233-260. 15 de diciembre 2013.
- ^ MIGEON, B (2010). "La inactivación del cromosoma X en las células humanas". La biomedicina y Ciencias de la vida colección. https://hstalks.com/?t=BL0132567): Henry Stewart habla, Ltd. pp. 1-54. 15 de diciembre 2013.
- ^ a b Gartler, Stanley M, Goldman, Michael (2001). "Inactivación del X-cromosoma" (PDF). Enciclopedia de Ciencias de la vida. www.Els.net: Nature Publishing Group. págs. 1 – 2. 10 de noviembre 2013.
- ^ Connallon, Tim, Clark, Andrew G (2013). "Selección diferencial de sexo y la evolución de la X inactivación estrategias". Enciclopedia de Ciencias de la vida. www.plosgenetics.org: revista PLOS Genetics. págs. 1 – 12. 15 de diciembre 2013.
- ^ Barakat, Tahsin Stefan. "Inactivación del cromosoma X y las células madre embrionarias".
- ^ Hoki Y Kimura N M Kanbayashi, Amakawa Y, Ohhata T, Sasaki H, Sado T (2009). "una próxima repetición conservada en el gene de Xist es esencial como elemento genómico para la inactivación de X en ratón". Desarrollo (Resumen) 136 (1): 139-46. doi:10.1242/dev.026427. PMID19036803.
- ^ K ng, Pullirsch D, Leeb M, Wutz A (2007). "Xist y la orden de silenciar" (Artículo de revisión). EMBO Rep 8 (1): 34 – 9. doi:10.1038/sj.embor.7400871. PMC1796754. PMID17203100.
Figura 1 Xist RNA comprende a la X de la que se transcribe.
- ^ Penny GD, Kay GF, Sheardown SA, S de Rastan, Brockdorff N (1996). "Requisito de Xist en la inactivación del cromosoma X". Naturaleza 379 (6561): 116-7. doi:10.1038/379131a0. PMID8538762.
- ^ a b Herzing LB, Romer JT, cuerno JM, Ashworth A (1997). "Xist tiene propiedades del centro de inactivación del cromosoma x". Naturaleza 386 (6622): 272 – 5. doi:10.1038/386272a0. PMID9069284.
- ^ Lee JT, Jaenisch R (1997). "efectos de largo alcance cis de ectópicos centros de inactivación de X en un autosome ratón". Naturaleza 386 (6622): 275 – 9. doi:10.1038/386275a0. PMID9069285.
- ^ Lee JT, Davidow LS, Warshawsky D (1999). "Tisx, un antisentido del gen que XIst en el centro de inactivación de X". NAT Genet 21 (4): 400 – 4. doi:10.1038/7734. PMID10192391.
- ^ K ng, Pullirsch D, Leeb M, Wutz A (2007). "Xist y la orden de silenciar" (Artículo de revisión). EMBO Rep 8 (1): 34 – 9. doi:10.1038/sj.embor.7400871. PMC1796754. PMID17203100.
Tabla 1 características de la inactiva X territorio
– Origina;
J de Chow, Yen Z, Ziesche S, Brown C (2005). "Silenciar del cromosoma de X mamífero". Annu Rev Genomics Hum Genet 6: 69-92. doi:10.1146/annurev.Genom.6.080604.162350. PMID16124854.
Lucchesi JC, Kelly WG, batea B (2005). "Cromatina remodelación en compensación de la dosis". Annu. Reverendo Genet. 39: 615 – 51. doi:10.1146/annurev.Genet.39.073003.094210. PMID16285873. - ^ C Costanzi, Pehrson JR (1998). "macroH2A1 de la histona se concentra en el cromosoma X inactivo de la hembra mamíferos". Naturaleza 393 (6685): 599-601. doi:10.1038/31275. PMID9634239.
- ^ C Costanzi, Stein P, Worrad DM, Schultz RM, Pehrson JR (2000). "MacroH2A1 de la histona se concentra en el cromosoma X inactivo de embriones de ratón preimplantacional femenino" (pdf). Desarrollo 127 (11): 2283-9. PMID10804171.
- ^ Barr ML, Bertram EG (1949). "Una distinción morfológica entre las neuronas de los hombres y mujeres y el comportamiento del satélite Nucleolar durante la síntesis de nucleoproteínas acelerado". Naturaleza 163 (4148): 676-7. doi:10.1038/163676a0. PMID18120749.
- ^ Plath K, S Mlynarczyk-Evans, Nusinow D, batea B (2002). "RNA de Xist y el mecanismo de inactivación del cromosoma X". Annu Rev Genet 36: 233-78. doi:10.1146/annurev.Genet.36.042902.092433. PMID12429693.
- ^ a b Carrel L, Willard H (2005). "Perfil de la x-inactivación revela amplia variabilidad en la expresión del gene X-ligado en hembras". Naturaleza 434 (7031): 400-404. doi:10.1038/nature03479. PMID15772666.
- ^ a b c Calabrese JM, sol W, canción L, Mugford JW, Williams L, Yee D, J Starmer, P Mieczkowski, Crawford GE, Magnuson T (2012). "Silenciamiento de elementos reguladores como un mecanismo de X inactivación específica". Célula 151 (5): 951-63. doi:10.1016/j.Cell.2012.10.037. PMID23178118.
- ^ a b Yang F, T de Babak, Shendure J, Disteche CM (2010). "Encuesta mundial de escape de X inactivación por secuenciación del RNA en el ratón". Investigación del genoma 20 (5): 614-22. doi:10.1101/gr.103200.109. PMID20363980.
- ^ Berletch JB, Yang F y Disteche CM (junio de 2010). "Escape de X inactivación en ratones y humanos". Biología del genoma 11 (6): 213. doi:10.1186/gb-2010-11-6-213. PMC2911101. PMID20573260.
- ^ Linder D: Gartler SM (octubre de 1965). "mosaicismo de glucosa-6-fosfato deshidrogenasa: utilización como marcador de la célula en el estudio de los leiomiomas". Ciencia 150 (3692): 67-9. doi:10.1126/Science.150.3692.67. PMID5833538.
- ^ Parsons, BL (2008). "muchos tipos de tumores diferentes tienen policlonal tumor origen: evidencia e implicaciones". Mutat Res 659: 232-247. doi:10.1016/j.mrrev.2008.05.004.
- ^ Chen, GL; Prchal, JT (2007). "Prueba de clonalidad de X-ligado: interpretación y limitaciones". Sangre 110: 1411-1419. doi:10.1182/sangre-2006-09-018655.
- ^ Petersson; et al. "el estroma leiomyomatous en carcinomas de células renales es policlonal y no forma parte del proceso neoplásico. Virchows Arch 465 (1): 89-96. doi:10.1007/s00428-014-1591-9.
- ^ Comertpay; et al (2014). "Evaluación de origen clonal del mesotelioma maligno". Revista de medicina traslacional 12: 301. doi:10.1186/s12967-014-0301-3.
- ^ Jiang; et al (2013). "Traducir la compensación de dosis a trisomía del par 21". Naturaleza 500:: 296-300. doi:10.1038/nature12394. PMC3848249. PMID23863942.
- Huynh KD, Lee JT (2005). "inactivación del X-cromosoma: una hipótesis entre ontogenia y filogenia". Naturaleza comentarios sobre genética 9 (5): 41 – 8. doi:10.1038/nrg1604. PMID15818384.
- Inactivación de X como causa posible para la autoinmunidad
Lectura adicional
Artículo de revisión
- T Goto, m. monje (01 de junio de 1998). "Regulación de la inactivación del X-cromosoma en desarrollo en ratones y humanos" (Artículo de revisión). Microbiol Mol Biol Rev 62 (2): 362 – 78. PMC98919. PMID9618446. 2009-03-18.
- M de Lyon (2003). El Lyon y la hipótesis de la línea. Semin Cell Dev Biol (Artículo de revisión) 14 (6): 313 – 8. doi:10.1016/j.semcdb.2003.09.015. PMID15015738.
- K ng, Pullirsch D, Leeb M, Wutz A (2007). "Xist y la orden de silenciar" (Artículo de revisión). EMBO Rep 8 (1): 34 – 9. doi:10.1038/sj.embor.7400871. PMC1796754. PMID17203100.
| Campos comunes de Wikimedia tiene medios relacionados con Inactivación del cromosoma x. |
Otras Páginas
- Euforia
- Comparacion de software de backup
- Dale Bumpers (abogados categoria de ciudad y ciudad en los Estados Unidos)
- Membrana del huevo
- Disfuncion somatica
- Stephan Schmidheiny
- Frank Cimorelli
- George Mathers, 1er Baron Mathers
- Shove hielo
- Informatica en salud (seccion comparacion entre de China estandar de EHR y segmentos de la norma ASTM E 1384)
- HTC Hero
- Samsung GT-E1150i
- Septiembre de 1972