Fluorescencia in situ hibridación
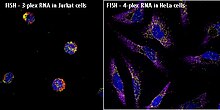

PESCADO (fluorescencia in situ hibridación) es una citogenéticos técnica desarrollada por investigadores biomédicos en los años 80 tempranos[1] se utiliza para detectar y localizar la presencia o ausencia de específicas DNA secuencias de en cromosomas. FISH utiliza sondas fluorescentes se unen a sólo aquellas partes del cromosoma con el que muestran un alto grado de secuencia complementariedad. Microscopía de fluorescencia puede utilizarse para averiguar donde la sonda fluorescente está ligada a los cromosomas. PESCADO se utiliza a menudo para encontrar características específicas en el ADN para su uso en la asesoría genética, la medicina y la identificación de las especies.[2] PESCADO también puede utilizarse para detectar y localizar específicos (objetivos) RNAmRNA, lncRNA y miRNA) en las células, circulación de las células tumorales y las muestras de tejido. En este contexto, puede ayudar a definir los patrones espaciales temporales de expresión del gen dentro de las células y tejidos.
Contenido
- 1 Sondas de ARN y ADN
- 1.1 Proceso de preparación y del hibridación RNA
- 1.2 Proceso de preparación y del hibridación ADN
- 1.3 Variaciones en puntas de prueba y análisis
- 1.4 Sondas QuantiGene ViewRNA ISH
- 1.5 Sondas de ARN pescado Stellaris(R)
- 1.6 Fibra pescado
- 1.7 Q-FISH
- 1.8 Flujo-pescado
- 2 Aplicaciones médicas
- 2.1 Identificación de especies
- 2.2 Hibridación Genomic comparativo
- 2.3 Cariotipo virtual
- 2.4 Cariotipo espectral
- 3 Véase también
- 4 Galería
- 5 Referencias
- 6 Lectura adicional
- 7 Enlaces externos
Sondas de ARN y ADN

Sondas de RNA pueden diseñarse para cualquier gen o cualquier secuencia dentro de un gen para la visualización del mRNA,[3][4][5] lncRNA[6][7][8] y miRNA en células y tejidos. PESCADO se utiliza examinando el ciclo de reproducción celular, específicamente la interfase de los núcleos de cualquier anormalidad cromosómica.[9] Esta técnica [pescado] permite el análisis de una serie grande de casos archivales mucho más fácil identificar el cromosoma identificó mediante la creación de una sonda con una base cromosómica artificial que atraerá a los cromosomas similares.[9] La hibridación de señales para cada sondeo cuando se detecta una anormalidad nucleico.[9] Cada punta de prueba para la detección de mRNA y lncRNA se compone de 20 pares de oligonucleótidos, cada par que cubre un espacio de 40-50 bp. Para la detección de miRNA, las sondas utilizan propiedad química para la detección específica de miRNA y cubren la secuencia entera de miRNA.

Puntas de prueba se derivan a menudo de fragmentos de ADN que fueron aislados, purificados y amplificados para el uso en la Proyecto genoma humano. El tamaño del genoma humano es tan grande, comparado con la longitud que puede ser secuenciada directamente, que era necesario dividir el genoma en fragmentos. (En el análisis final, estos fragmentos fueron puestos en orden por digerir una copia de cada fragmento en fragmentos aún más pequeños utilizando endonucleasas específicas de secuencia, medir el tamaño de cada pequeño fragmento utilizando Cromatografía por exclusión de tamañoy utilizando esa información para determinar donde los grandes fragmentos superpuestos uno a otro.) Para conservar los fragmentos con sus secuencias individuales de la DNA, los fragmentos fueron agregados en un sistema de reproducir continuamente las poblaciones de bacterias. Población clonal de las bacterias, cada población manteniendo un solo cromosoma artificial, se almacena en varios laboratorios alrededor del mundo. El (cromosomas artificialesBAC) puede crecido, extraídos y marcados, en cualquier laboratorio. Estos fragmentos son del orden de 100 mil pares de bases y que puntas de prueba de la base para la mayoría de los peces.
Proceso de preparación y del hibridación RNA
Células, las células tumorales circulantes (CTC), o parafina-encajado formalina-fijos (FFPE) o secciones congeladas del tejido son fijos, entonces permeabilized para permitir la accesibilidad del destino. PESCADO también se ha hecho con éxito en células no fijadas.[10] Un sondeo específico del destino, compuesto de 20 pares de oligonucleótidos, hibridiza en el destino del RNA(s). Sistemas de amplificación de señal independientes pero compatibles permiten el ensayo multiplex (hasta dos objetivos por ensayo). Amplificación de la señal se consigue mediante una serie de pasos secuenciales de la hibridación. Al final del ensayo se visualizan las muestras de tejido bajo un microscopio de fluorescencia.
Proceso de preparación y del hibridación ADN

En primer lugar, se construye una sonda. La sonda debe ser lo suficientemente grande para hibridar específicamente con su objetivo, pero no tan grande como para impedir el proceso de hibridación. La sonda es con la etiqueta directamente con fluoróforos, con objetivos para anticuerpos o con biotina. Etiquetado puede hacerse de varias maneras, tales como traducción de Nick, o POLIMERIZACIÓN EN CADENA usando la etiqueta nucleótidos.
Entonces, un interfase o metafase preparación de cromosomas se produce. Los cromosomas se unen firmemente a una sustrato, generalmente de cristal. Secuencias de ADN repetitivas deben bloquearse mediante la adición de fragmentos cortos de ADN a la muestra. La punta de prueba entonces se aplica al cromosoma ADN e incubado durante aproximadamente 12 horas al cruzamiento por hibridación. Varios pasos de lavado retirar todas las sondas de unhybridized o parcialmente hibridadas. Los resultados son entonces visualizaron y cuantificaron utilizando un microscopio que sea capaz de excitar el tinte y grabación de imágenes.
Si la señal fluorescente es débil, la amplificación de la señal puede ser necesaria para superar el umbral de detección de la microscopio. Intensidad de la señal fluorescente depende de muchos factores tales como sonda de etiquetado de eficiencia, el tipo de sonda y el tipo de tinte. Etiquetado fluorescente anticuerpos o estreptavidina están enlazados a la molécula del tinte. Estos componentes secundarios son seleccionados para que tengan una señal fuerte.
Variaciones en puntas de prueba y análisis

El pescado es una técnica muy general. Las diferencias entre las distintas técnicas de pesca son generalmente debido a variaciones en la secuencia y el etiquetado de las sondas; ¿y cómo se utilizan en combinación. Puntas de prueba se dividen en dos categorías genéricas: celular y acelular. "In situ" en fluorescencia hibridación in situ se refiere a la colocación de la sonda colocada cellularly.[11]
Tamaño de la sonda es importante porque más sondas hibridan menos específicamente que las puntas de prueba más cortos, "un filamento corto de ADN o ARN (a menudo 10 a 25 nucleótidos) que es complementario a una secuencia dada, puede utilizarse para identificar o localizar el blanco.". El traslapo define la resolución de características perceptibles. Por ejemplo, si el objetivo de un experimento es detectar el punto de interrupción de un desplazamiento, entonces la superposición de las sondas, el grado al que una ADN secuencia figura en los sondeos adyacentes — define la mínima ventana en la que se puede detectar el punto de interrupción.
La mezcla de secuencias sonda determina el tipo de función de que la sonda puede detectar. Sondas que hibridan a lo largo de un cromosoma entero se utilizan para contar el número de un determinado cromosoma, muestran desplazamientos o identificar fragmentos extra cromosómicos de cromatina. Esto se denomina "cromosoma de toda pintura." Si se utiliza cada sonda posible, cada cromosoma (el genoma) se estaría marcado fluorescente, que no sería particularmente útil para determinar características de secuencias individuales. Sin embargo, es posible crear una mezcla de pequeñas sondas que son específicos a una región particular (locus) de ADN; Estas mezclas se utilizan para detectar mutaciones de la canceladura. Cuando se combina con un color específico, se utiliza una mezcla de sonda de locus específico para detectar desplazamientos muy concretos. Sonda especial de locus específico las mezclas a menudo se utilizan para contar los cromosomas, atando a la centromérica regiones de los cromosomas, que son suficientemente distintivos para identificar cada cromosoma (con la excepción de Cromosoma 13, 14, 21, 22.)
Una variedad de otras técnicas de utilizar mezclas de sondas de diferente colores. Una gama de colores en mezclas de tintes fluorescentes puede ser detectada, por lo que cada cromosoma humano puede identificarse por un color característico utilizando mezclas de sonda de cromosoma entero y una variedad de cocientes de colores. Aunque hay más cromosomas de colores fácilmente distinguibles de colorante fluorescente, proporciones de las mezclas de la punta de prueba pueden utilizarse para crear secundaria colores. Similar a la hibridación genomic comparativo, se crea la mezcla de sonda para los colores secundarios mezclando la proporción correcta de dos conjuntos de sondas de diferente colores para el mismo cromosoma. Esta técnica es a veces llamado M-FISH.
La misma física que posibilitan una gran variedad de colores de M-FISH puede ser utilizada para la detección de translocaciones. Es decir, colores que son adyacentes parecen superponerse; se observa un color secundario. Algunos ensayos están diseñados para que el color secundario será presentes o ausentes en los casos de interés. Un ejemplo es la detección de BCR/ABL translocaciones, donde el color secundario indica enfermedad. Esta variación se denomina doble fusión peces o D. En la situación opuesta, donde la ausencia del color secundario es patológica, es ilustrado por un ensayo utilizado para investigar los desplazamientos donde sólo uno de los puntos de interrupción se conoce o constante. Sondas de locus específico se hacen para un lado del punto de desempate y el otro cromosoma intacto. En las células normales, se observa el color secundario, pero sólo los colores primarios se observan cuando se produce el desplazamiento. Esta técnica se denomina 'break-apart pez'.
Sondas QuantiGene ViewRNA ISH
Sondas QuantiGene ViewRNA ISH es un método de detección y cuantificación de moléculas de mRNA, lncRNA y miRNA en muestras de tejido que son FFPE (formalina-fijo parafina-encajados), frescos, o congelados y en muestras de células y las células tumorales circulantes (CTC). ISH ViewRNA sondas permiten sensibilidad de RNA molécula única con prácticamente ningún fondo. Cada punta de prueba (para la detección de mRNA y lncRNA) se compone de 20 pares de oligonucleótidos. Cada par de oligo forma una plataforma necesaria para el montaje de la estructura de amplificación de señal (árbol) a través de una serie de pasos secuenciales hibridación utilizando la tecnología de amplificación de señal de ADN (bDNA) ramificada. Cada estructura completamente montado, cubre un espacio de 40-50 bit/s de la meta ARNm/lncRNA, y tiene la capacidad de amplificación de la señal 400-fold. Por lo tanto, un sondeo específico destino típico (contiene 20 pares de oligo) tiene la capacidad de generar 8,000-fold amplificación de la señal. Independiente pero sistemas de amplificación de señal compatible permiten la detección simultánea de hasta cuatro destino mRNAs/lncRNAs en las células/CTC y dos mRNAs/lncRNAs en los tejidos.
Sondas de ARN pescado Stellaris(R)
Stellaris ARN pescado, anteriormente conocido como sola molécula ARN FISH, es un método de detección y cuantificación de ARNm y otras largas moléculas de ARN en una capa delgada de la muestra de tejido. Objetivos pueden ser confiablemente reflejadas a través de la aplicación de múltiples Resumen individualmente etiquetados sondas de oligonucleótidos.[12] La Unión de hasta 48 etiquetada fluorescente oligos para una sola molécula de ARNm proporciona suficiente fluorescencia para detectar con precisión y localizar cada uno blanco mRNA en un amplio campo Microscopía fluorescente imagen. Sondas no vinculante a la secuencia prevista no consigue suficiente fluorescencia localizada para distinguirse de Fondo.[13]
Una sola molécula ARN pescado ensayos pueden realizarse en simplex o MULTIPLEXy puede ser utilizado como un experimento de seguimiento para PCR cuantitativa, o imagen simultáneamente con un anticuerpo fluorescente ensayo. La tecnología tiene potenciales aplicaciones en diagnóstico de cáncer,[14] Neurociencia, expresión del gen Análisis,[15] y Diagnostico de compañero.
Fibra pescado
En una técnica alternativa a la interfase o preparaciones en metafase, fibra pescado, interfase los cromosomas se unen a una diapositiva de tal forma que se estiró en una línea recta, en lugar de ser firmemente enrollada, como pescado convencional, o la adopción de un territorio del cromosoma conformación, como en pescados de la interfase. Esto se logra mediante la aplicación mecánica esfuerzo cortante a lo largo de la longitud de la diapositiva, o bien a células que han sido fijadas a la diapositiva y, a continuación lisis, o a una solución de DNA purificado. Una técnica conocida como cromosoma para peinar es cada vez más utilizado para este propósito. La conformación extendida de los cromosomas permite dramáticamente mayor resolución – incluso hasta unos cuantos kilobases. La preparación de muestras de pescados de la fibra, aunque conceptualmente simple, es un arte más bien cualificado, y sólo laboratorios especializados utilizan rutinariamente la técnica.
Q-FISH
Q-FISH combina el pescado con PNAs y software de computadora para cuantificar la intensidad de la fluorescencia. Esta técnica se utiliza habitualmente en telómero investigación de longitud.
Flujo-pescado
Flujo-pescado utiliza Citometría de flujo para realizar el pescado automáticamente utilizando mediciones de la fluorescencia por celda.
Aplicaciones médicas
A menudo los padres de niños con un discapacidades del desarrollo ¿quiere saber más acerca de las condiciones de su hijo antes de elegir tener otro hijo. Estos problemas pueden abordarse mediante el análisis de los padres y del niño ADN. En los casos donde no se entiende la discapacidad en el desarrollo del niño, la causa de puede potencialmente ser determinada mediante peces y citogenéticos técnicas. Ejemplos de enfermedades que se diagnostican con pescado Síndrome de Prader-Willi, Síndrome de Angelman, síndrome de la canceladura 22q13, leucemia mielógena crónica, leucemia linfoblástica aguda, CRI-du-chat, Síndrome de Velocardiofacial, y Síndrome de Down. PECES en células de la esperma está indicado para hombres con un anormal somáticos o meióticas karyotype así como aquellos con oligozoospermia, ya que aproximadamente el 50% de los hombres oligozoospermic tienen una tasa mayor de anormalidades del cromosoma del esperma.[16] El análisis de los cromosomas 21, X e Y es suficiente para identificar a individuos oligozoospermic con riesgo.[16]
En medicina, pescado puede utilizarse para formar un diagnóstico, para evaluar pronóstico, o para evaluar remisión de una enfermedad, tales como cáncer. Tratamiento de continuación puede ser adaptado específicamente. Un examen tradicional que implica el análisis del cromosoma metafase a menudo es incapaz de identificar características que distinguen a una enfermedad de otro, debido a las características cromosómicas sutiles; PESCADO puede aclarar estas diferencias. PESCADO también puede utilizarse para detectar las células enfermas más fácilmente que el estándar Citogenéticos métodos, que requieren dividir las células y requiere trabajo y tiempo-intensivo preparación manual y análisis de las diapositivas por un tecnólogo. PESCADO, por otro lado, no requieren de células vivas y puede ser cuantificada automáticamente, cuenta con una computadora los puntos fluorescentes presentes. Sin embargo, un tecnólogo entrenado es necesaria para distinguir las diferencias sutiles en patrones de bandeo en cromosomas en metafase doblado y torcido. PECES pueden ser incorporados en Lab-on-a-chip dispositivo de microfluidos. Esta tecnología está todavía en una etapa de desarrollo pero, como otro laboratorio sobre los métodos de un chip, puede conducir a las técnicas de diagnóstico más portátiles.[17][18]
Identificación de especies
PESCADO se utiliza a menudo en estudios clínicos. Si un paciente está infectado con un sospechoso patógeno, bacterias, tejidos o líquidos, el paciente normalmente se cultivan en agar para determinar la identidad del patógeno. Muchas bacterias, sin embargo, incluso especies bien conocidas, no crecen bien bajo condiciones de laboratorio. PESCADO puede utilizarse para detectar directamente la presencia del sospechoso en pequeñas muestras de tejido del paciente.
PESCADO también puede utilizarse para comparar los genomas de dos biológicos especies, deducir evolutiva relaciones. Una técnica similar de hibridación se llama un blot de Zoo. Sondas FISH bacterianas son a menudo cartillas para la 16S rRNA región.
PESCADO es ampliamente utilizado en el campo de la Ecología microbiana, para identificar microorganismos. Biofilms, por ejemplo, están compuestos de complejas organizaciones bacterianas (a menudo) de varias especies. Preparación de ADN sondas de una sola especie y realizar pesca con esta sonda permite visualizar la distribución de esta especie específica dentro de la biopelícula. Preparación de puntas de prueba (en dos colores diferentes) para las dos especies permite para visualizar/estudio de colocalización de estas dos especies en el biofilm y puede ser útil en la determinación de la fina arquitectura de la biopelícula.
Hibridación Genomic comparativo
Hibridación genomic comparativo puede ser descrito como un método que utiliza pescado en forma paralela con la comparación de la fuerza de hibridación para recordar grandes interrupciones en el proceso de duplicación de las secuencias de ADN en el genoma del núcleo.[19]
Cariotipo virtual
Cariotipo virtual otra alternativa rentable, clínicamente disponible para paneles de peces utiliza miles de millones de sondas en una sola matriz para detectar cambios números de copia, todo el genoma, a una resolución sin precedentes. Actualmente, este tipo de análisis sólo detecta ganancias y pérdidas de material cromosómico y no detecta reordenamientos balanceados, tales como translocaciones e inversiones que son aberraciones de la seña de identidad en muchos tipos de leucemia y linfoma.
Cariotipo espectral
Karyotyping espectral es una imagen de cromosomas coloreados. Karyotyping espectral consiste en pescado con múltiples formas de muchos tipos de sondas el resultado para ver cada cromosoma marcada por su etapa de metafase. Este tipo de cariotipo se utiliza específicamente cuando buscan acuerdos de cromosoma.
Véase también
| Campos comunes de Wikimedia tiene medios relacionados con Hibridación fluorescente in situ. |
- Hibridación in situ, la técnica utilizada para el etiquetado
- Hibridación in situ cromogénico (CISH)
- Citogenética molecular
- Cariotipo virtual
- Asignación de feliz
Galería
-

Otro esquema de proceso de pescado.
-

Chip de microfluidos que baja el costo por prueba de peces en un 90%.
-

Imagen de pez doble etiqueta; Bifidobacterias Cy3, bacterias totales FITC.
Referencias
- ^ Langer-más seguro, p. R.; Levine, m..; Ward, C. D. (1982). "Método inmunológico para el mapeo de genes en Drosophila politenizadas cromosomas". Actas de la Academia Nacional de Ciencias 79 (14): 4381. Bibcode:1982PNAS... 79,4381 L. doi:10.1073/pnas.79.14.4381. PMC346675. PMID6812046.
- ^ Amann, Rudolf; Fuchs, Bernhard M. (2008). "Identificación de unicelular en comunidades microbianas por fluorescencia mejorada in situ técnicas de hibridación". Naturaleza comentarios microbiología 6 (5): 339-348. doi:10.1038/nrmicro1888.
- ^ Anthony, J.; St. Leger, j. A.; Pugliares, K.; IP, H. S.; Chan, J. M.; Carpintero, Z. W.; Navarrete Macias, I.; Sánchez León, m..; Saliki, T. J.; Pedersen, J.; Karesh, w el.; Daszak, P.; Rabadan, R.; Rowles, T.; Lipkin, W. I. (2012). "Aparición de la gripe aviar Fatal en focas de Nueva Inglaterra". MBio 3 (4): e00166-e00112. doi:10.1128/mBio.00166-12. PMC3419516. PMID22851656.
- ^ Everitt, A. R.; Clare, S.; Pertel, T.; John, S. P.; Lavado, R. S.; Smith, S. E.; Chin, C. R.; Feeley, m. e.; Sims, J. S.; Adams, J. D.; Sabio, H. M.; Kane, L.; Goulding, D.; Digard, P.; Anttila, V.; Baillie, j. K.; Walsh, T. S.; Hume, D. A.; Palotie, A.; Xue, Y.; Colonna, V.; Tyler-Smith, C.; Dunning, J.; Gordon, S. B.; Everingham, K.; Dawson, H.; Esperanza, D.; Ramsay, p.; Walsh (investigador principal Local), T. S. et al (2012). "IFITM3 restringe la morbilidad y mortalidad asociada con la influenza". Naturaleza 484 (7395): 519. Bibcode:2012Natur.484... 519. doi:10.1038/nature10921. PMID22446628.
- ^ Louzada, S.; Adega, f el.; Chaves, R. (2012). "Definir la hermana rata tumor mamario célula líneas HH-16 cl.2/1 y HH-16.cl.4 como un en vitro modelo de célula para ErbB2". PLoS uno 7 (1): e29923. Bibcode:2012PLoSO... 729923L. doi:10.1371/journal.pone.0029923. PMC3254647. PMID22253826.
- ^ Ting, T. D.; Lipson, D.; Pablo, S.; Brannigan, W. B.; Akhavanfard, S.; Coffman, e. J.; Contino, G.; Deshpande, V.; Iafrate, A. J.; Letovsky, S.; Rivera, M. N.; Bardeesy, N.; Maheswaran, S.; Haber, D. A. (2011). «Sobreexpresión aberrante del satélite repite en páncreas y otros cánceres epiteliales». Ciencia 331 (6017): 593. Bibcode:2011Sci... 331..593T. doi:10.1126/Science.1200801. PMID21233348.
- ^ Zhang, B.; Arun, G.; Mao, Y. S.; Lazar, Z.; Hung, G.; Bhattacharjee, G.; Xiao, X.; Booth, C. J.; Wu, J.; Zhang, C.; Spector, D. L. (2012). «LncRNA Malat1 es prescindible para el desarrollo del ratón pero su transcripción juega un papel regulador en cis en el adulto». Informes celular 2 (1): 111-23. doi:10.1016/j.celrep.2012.06.003. PMC3408587. PMID22840402.
- ^ Lee, K.; Kunkeaw, N.; Jeon, S. H.; Lee, I.; Johnson, H. B.; Kang, g. -Y.; Bang, J. Y.; Park, S. H.; Leelayuwat, C.; Lee, S. Y. (2011). Precursor miR-886, un novela RNA noncoding reprimido en el cáncer, se asocia con PKR y modula su actividad. RNA 17 (6): 1076. doi:10.1261/RNA.2701111. PMID21518807.
- ^ a b c Bernasconi, B.; Karamitopolou-Diamantiis, E.; Tornillo, L.; LUGLi, A.; Di Vizio, D.; Dirnhofer, S.; Wengmann, S.; Glatz-Krieger, K.; Fend, f el.; Capella, C.; Insabato, L.; Terracciano, L. M. (2008). "Inestabilidad cromosómica en los linfomas de tejido linfoide asociado a mucosa gástrica: un estudio de hibridación in situ fluorescente utilizando un enfoque de microarray de tejido". Patología humana 39 (4): 536-42. doi:10.1016/j.humpath.2007.08.009. PMID18234275.
- ^ Haroon, Mohamed f, Skennerton, Connor T., Steen, Jason A., Lachner, Nancy, Hugenholtz, Philip y Tyson, Gene W. (2013). "Capítulo en uno – fluorescencia en solución en hibridación del Situ y clasificación celular activado por fluorescencia de unicelular y recuperación de genoma de población". En f el. DeLong Edward. Métodos en enzimología 531. Academic Press. págs. 3 – 19.
- ^ Camesano, Terri A. y Mello, Charlene M. (2008). Serie del Simposio de ACS. American Chemical Society. ISBN9780841274303.
- ^ Raj, A.; Van Den Bogaard, P.; Rifkin, S. A.; Van Oudenaarden, A.; Tyagi, S. (2008). "Imágenes individuales moléculas de mRNA usando múltiples individualmente etiquetados como sondas". Métodos de naturaleza 5 (10): 877. doi:10.1038/nmeth.1253. PMID18806792.
- ^ Biosearch tecnologías signos licencia exclusivo para tecnologías de pescado sola molécula de UMDNJ. biosearchtech.com
- ^ "Una nueva prueba para el cáncer de Colon recurrente". Anales de medicina interna 131 (11): 805. 1999. doi:10.7326/0003-4819-131-11-199912070-00024.
- ^ Kosman, D.; Mizutani, C. M.; Limones, D; Cox, G. W.; McGinnis, W; Bier, E (2004). "Detección multiplex de expresión de ARN en embriones de Drosophila". Ciencia 305 (5685): 846. doi:10.1126/Science.1099247. PMID15297669.
- ^ a b Sarrate, Z.; Vidal, f.; Blanco, J. (2010). "Estudios de papel de la hibridación in situ fluorescente de espermatozoides en pacientes infértiles: indicaciones, estudio enfoque y relevancia clínica". Fertilidad y esterilidad 93 (6): 1892. doi:10.1016/j.fertnstert.2008.12.139. PMID19254793.
- ^ Kurz, C. M.; v.d. Moosdijk, S.; Thielecke, H.; Velten, T. (2011). "Hacia una plataforma celular de múltiples parámetros de análisis: fluorescencia in situ hibridación (pescado) en microhole arreglos". 2011 Conferencia Internacional anual de la ingeniería de IEEE en la sociedad de biología y medicina. p. 8408. doi:10.1109/IEMBS.2011.6092074. ISBN978-1-4577-1589-1.
- ^ Eneldo, K., Hui Liu, R., Grodzinski, P. (2008). Microarrays: Preparación, microfluídica, métodos de detección y usos biológicos. Springer. p. 323. ISBN0387727167.
- ^ "Hibridación genómica comparativa". McGraw-Hill Diccionario de términos científicos y técnicos. 19 de septiembre 2013.
Lectura adicional
- Pernthaler A, J Pernthaler, Amann R (2002). "Fluorescencia In Situ hibridación y deposición de reportero catalizado para la identificación de bacterias marinas". Microbiología aplicada y ambiental 68 (6): 3094-3101. doi:10.1128/AEM.68.6.3094-3101.2002. PMC123953. PMID12039771.
- Wagner M, cuerno M, Daims H (2003). "Fluorescencia hibridación in situ para la identificación y caracterización de los procariotas". Opinión actual en Microbiología 2003 (6): 302 – 309. doi:10.1016/S1369-5274 (03) 00054-7.
- Carthy, J.D. (1965). Puntos de vista en biología. Inglaterra: Butterworth & Co. p. 66.
Enlaces externos
- Hibridación fluorescente in Situ en las Estados Unidos Biblioteca Nacional de medicina Encabezamientos de temas médicos (MeSH)
- Información sobre la fibra pescado desde el Olympus Corporation
- A Guía de fibra pescado de Octavian Henegariu
- Protocolo de pesca de fibra desde el Proyecto genoma humano en el Centro de Sanger
- CARD-FISH, BioMineWiki
- Preparación de complejos conjuntos de ADN sonda para pesca 3D con hasta seis diferentes fluorocromos
- PESCADO de notas técnicas y protocolos de GeneDetect.com
- Fluorescencia in situ hibridación fotos de bacterias
- Diseño racional de mezclas de Polinucleótido sonda para identificar genes particulares en define taxones: www.dnaBaser.com/PolyPro
|
||||||||||||||||||
Otras Páginas
- Nokia (redireccion de telefono Nokia)
- Registro de sangre de cordon
- North Lawndale, Chicago (areas de la comunidad de la categoria de Chicago, Illinois)
- LeeMon
- Cataplasmas
- Cuenta de ahorros medico (Estados Unidos)
- Darapsa Myron
- Canada salud Infoway
- Max Hardberger (escritores de maritimo de categoria)
- Lecomte (arquero)
- A. C. Bhaktivedanta Swami Prabhupada
- Red de alerta de salud


