Desorden congénito del glycosylation
| Trastornos congénitos de la glicosilación | |
|---|---|
| Clasificación y recursos externos | |
| CIE-10 | E77.8 |
| CIE-9 | 271.8 |
| OMIM | 212065 212066 |
| DiseasesDB | 2012 31730 |
A desorden congénito del glycosylation (síndrome de glicoproteína con deficiencia de carbohidrato anteriormente llamada) es uno de los varios raros errores innatos del metabolismo en el cual glicosilación de una variedad de tejido proteínas o lípidos es deficiente o defectuosa. Trastornos congénitos de glicosilación se conocen a veces como CDG síndromes. A menudo causan grave, a veces fatal, mal funcionamiento de diversos sistemas del órgano (especialmente la sistema nervioso, músculos, y intestinos) en los niños afectados. El subtipo más común es CDG-Ia (también denominado PMM2-CDG) donde el defecto genético conduce a la pérdida de phosphomannomutase 2, la enzima responsable de la conversión de manosa-6-fosfato en manosa-1-fosfato.
Contenido
- 1 Historia
- 2 Clasificación
- 2.1 Tipo I
- 2.2 Tipo II
- 2.3 Trastornos de O-mannosylation
- 3 Presentación
- 4 N-Glicosilación y defectos conocidos
- 4.1 Tipo I
- 4.2 Tipo II
- 5 Tratamiento
- 6 Véase también
- 7 Referencias
- 8 Enlaces externos
Historia
Los primeros pacientes CDG (hermanas gemelas) fueron descritos en un extracto en la revista médica Pediatric Research en 1980 por Jaeken et al.[1] Sus características principales eran retraso psicomotor, cerebral y atrofia cerebelosa y fluctuante hormona los niveles)por ejemploprolactina, FSH y GH). Durante los próximos 15 años que el defecto subyacente permanece desconocido, pero desde el plasmaprotein transferrina fue underglycosylated (como se muestra por ejemplo isoeléctrica), el nuevo síndrome fue denominado síndrome de glicoproteína con deficiencia de carbohidrato (CDG).[2] Su "clásico" fenotipo incluido retraso psicomotor, ataxia, estrabismo, anomalías (almohadillas de grasa e invertida pezones) y coagulopatía.
En 1994, un nuevo fenotipo fue descrito y había nombrado CDGS-II.[3] En 1995, Van Schaftingen y Jaeken mostraron que CDGS-yo (ahora CDG-Ia o PMM2-CDG) estaba causada por la deficiencia de la enzima phosphomannomutase. Esta enzima es responsable de la interconversión de manosa-6-fosfato y manosa-1-fosfato, y su deficiencia conduce a una escasez en PIB-manosa y Dolicol (Dol)-manosa (Hombre), los dos donantes necesaria para la síntesis del precursor del lípido-ligado oligosacárido de glicosilación N-ligados.
En 1998, Niehues et al publicaron un nuevo síndrome CDG, CDG-Ib, que es causado por mutaciones en la enzima metabólicamente aguas arriba del PMM2, phosphomannose isomerase (PMI).[4] En este documento, los autores también describieron una terapia funcional para CDG-Ib, manosa alimentario.
La caracterización de nuevos defectos tomó velocidad y varios nuevo tipo I y tipo II defectos estábamos delineados.[5]
En 2012, necesidad et al publicaron el primer caso de un desorden congénito del deglycosylation, que resultó de las mutaciones en el NGLY1 Gene.[6] Un estudio de 2014 NGLY1 los pacientes deficientes encontraron similitudes con tradicionales trastornos congénitos de la glicosilación.[7]
Clasificación
Históricamente, CDGs se clasifican como tipo I y II (CDG-I y II-CDG), dependiendo de la naturaleza y la localización del defecto bioquímico en la vía metabólica relativa a la acción de oligosaccharyltransferase. El método de cribado más comúnmente utilizado para CDG, análisis de situación de glicosilación de transferrina por isoeléctrica, ESI-MS, u otras técnicas, distinguir entre estos subtipos en llamados tipo I y tipo II patrones.
En la actualidad, veintidós CDG tipo-catorce subtipos del tipo II de CDG y hemos descritos.[8]
Desde 2009, la mayoría de los investigadores utilizan una nomenclatura diferente basada en el gen defecto (por ejemplo CDG-Ia = PMM2-CDG, CDG-Ib = PMI-CDG, CDG-Ic = ALG6-CDG, etc..).[9] El motivo de la nueva nomenclatura fue el hecho de que las proteínas no directamente implicadas en la síntesis glicanos (como los miembros de la familia COG[10] y vesicular H +-ATPasa [11]) fueron encontrados para ser la causa del defecto de glicosilación en algunos pacientes CDG.
Además, defectos molestar a otras vías de glicosilación de la N-vinculado son incluidos en esta clasificación. Los ejemplos son la α-distroglicanopatías (por ejemplo (POMT1/POMT2-CDGSíndrome de Walker-Warburg y Síndrome músculo-ojo-cerebro)) con deficiencias en O-mannosylation de las proteínas; Odefectos de síntesis - xylosylglycan (EXT1/EXT2-CDG)hereditario exostosis múltiples) y (B4GALT7-CDGSíndrome de Ehlers-Danlosvariante del progeroid)); Osíntesis - fucosylglycan (B3GALTL-CDG (Peter más síndrome) y (LFNG-CDGDisostosis espondilocostal III)).
Tipo I
- Tipo I trastornos implican interrumpida la síntesis de la lípidos-vinculadas oligosacárido precursor (LLO) o su transferencia a la proteína.
Los tipos incluyen:
| Tipo | OMIM | Gene | Lugar geométrico |
|---|---|---|---|
| Ia (PMM2-CDG) | 212065 | PMM2 | 16p13.3-p13.2 |
| IB (MPI-CDG) | 602579 | MPI | 15q22-qter |
| IC (ALG6-CDG) | 603147 | ALG6 | 1p22.3 |
| ID (ALG3-CDG) | 601110 | ALG3 | 3q27 |
| IE (DPM1-CDG) | 608799 | DPM1 | 20q13.13 |
| Si (MPDU1-CDG) | 609180 | MPDU1 | 17p13.1-p12 |
| IG (ALG12-CDG) | 607143 | ALG12 | 22q13.33 |
| IH (ALG8-CDG) | 608104 | ALG8 | 11pter-p15.5 |
| II (ALG2-CDG) | 607906 | ALG2 | 9q22 |
| Ij (DPAGT1-CDG) | 608093 | DPAGT1 | 11q23.3 |
| Ik (ALG1-CDG) | 608540 | ALG1 | 16p13.3 |
| 1L (ALG9-CDG) | 608776 | ALG9 | 11q23 |
| Im (DOLK-CDG) | 610768 | DOLK | 9q34.11 |
| En (RFT1-CDG) | 612015 | RFT1 | 3p21.1 |
| Io (DPM3-CDG) | 612937 | DPM3 | 1T12-q21 |
| IP (ALG11-CDG) | 613661 | ALG11 | 13q14.3 |
| IQ (SRD5A3-CDG) | 612379 | SRD5A3 | 4q12 |
| Ir (DDOST-CDG) | 614507 | DDOST | 1p36.12 |
| DPM2-CDG | n / a | DPM2 | 9q34.13 |
| TUSC3-CDG | 611093 | TUSC3 | 8 22 p |
| MAGT1-CDG | 300716 | MAGT1 | X21.1 |
| DHDDS-CDG | 613861 | DHDDS | 1p36.11 |
| Me / IIx | 212067 | n / a | n / a |
Tipo II
- Tipo II trastornos implican recorte/procesamiento de mal funcionamiento de la cadena unida a las proteínas oligosacárido.
Los tipos incluyen:
| Tipo | OMIM | Gene | Lugar geométrico |
|---|---|---|---|
| IIa (MGAT2-CDG) | 212066 | MGAT2 | 14q21 |
| IIb (GCS1-CDG) | 606056 | GCS1 | 2p 13-p12 |
| CII (SLC335C1-CDG; Deficiencia del leucocito adherencia II)) | 266265 | SLC35C1 | 11p11.2 |
| IId (B4GALT1-CDG) | 607091 | B4GALT1 | 9 13 p |
| IIe (COG7-CDG) | 608779 | COG7 | 362 |
| IIf (SLC35A1-CDG) | 603585 | SLC35A1 | 6q15 |
| IIg (COG1-CDG) | 611209 | COG1 | 17q25.1 |
| IIh (COG8-CDG) | 611182 | COG8 | 16q22.1 |
| IIi (COG5-CDG) | 613612 | COG5 | 7q31 |
| IIj (COG4-CDG) | 613489 | COG4 | 16q22.1 |
| IIL (COG6-CDG) | n / a | COG6 | 13q14.11 |
| ATP6V0A2-CDG (autosómico recesivo cutis laxa tipo 2a (ARCL-2A)) | 219200 | ATP6V0A2 | 12q24.31 |
| MAN1B1-CDG (Retraso Mental, 15 autosómico recesivo) | 614202 | MAN1B1 | 9q34.3 |
| ST3GAL3-CDG (Retraso Mental, 12 autosómico recesivo) | 611090 | ST3GAL3 | 1p34.1 |
Trastornos de O-mannosylation
- Trastornos con deficiente α-dystroglycan O-mannosylation.
Las mutaciones en varios genes han sido asociadas con los síndromes clínicos tradicionales, denominados distrofia muscular-distroglicanopatías (MDDG). OMIM propuso recientemente una nueva nomenclatura basada en la severidad clínica y causa genética.[12] Las clasificaciones de gravedad son un (grave), B (intermedio) y C (suave). Los subtipos están contados uno a seis, según la causa genética, en el orden siguiente: (1) POMT1, (2) POMT2, (3) POMGNT1, (4) FKTN, (5) FKRPy (6) GRANDE.
Tipos severos más comunes incluyen:
| Nombre | OMIM | Gene | Lugar geométrico |
|---|---|---|---|
| POMT1-CDG (MDDGA1;Síndrome de Walker-Warburg) | 236670 | POMT1 | 9q34.13 |
| POMT2-CDG (MDDGA2;Síndrome de Walker-Warburg) | 613150 | POMT2 | 14q24.3 |
| POMGNT1-CDG (MDDGA3; músculo-ojo-cerebro) | 253280 | POMGNT1 | 1p34.1 |
| FKTN-CDG (MDDGA4; Distrofia muscular congénita de Fukuyama) | 253800 | FKTN | 9q31.2 |
| FKRP-CDG (MDDGB5; MDC1C) | 606612 | FKRP | 19q13.32 |
| GRANDE-CDG (MDDGB6; MDC1D) | 608840 | GRANDE | 22q12.3 |
Presentación
Los problemas específicos que producen difieren según la particular síntesis anormal involucrada. Las manifestaciones comunes incluyen ataxia; convulsiones; retinopatía; hígado fibrosis; coagulopatías; falta de prosperar; rasgos dismórficos (por ejemplo, pezones invertidos y subcutánea cojines gordos; y estrabismo. Si se obtiene un MRI, hipoplasia y atrofia cerebelosa es un hallazgo común.
Las anormalidades oculares de CDG-Ia incluyen: miopía, esotropía infantil, retrasa la maduración visual, baja visión, palidez del disco ópticoy la reducción barra función de Electrorretinografía.[13]
Tres subtipos de CDG I (a, b, d) pueden causar hiperinsulinismo con hipoglucemia hyperinsulinemic en la infancia.[14]
N-Glicosilación y defectos conocidos
Un grupo biológicamente muy importante de hidratos de carbono es el Asparagina (ASN)-ligado, o N-ligados, oligosacáridos. Sus camino biosintético es muy complejo e involucra un centenar o más glicosiltransferasas, glicosidasas, Transportadores y Sintasas. Esta plétora permite la formación de una multitud de estructuras diferentes oligosacárido final, envueltas en plegamiento de la proteína, intracelular transporte y localización, actividad de la proteína y degradación/half-life. Una gran cantidad de hidratos de carbono vinculante (moléculaslectinas) dependen de glicosilación correcta para el enlace adecuado; el selectins, involucrados en leucocito extravasación, es un buen ejemplo. Su enlace depende de una correcta fucosylation de superficie de la célula glicoproteínas. Su ausencia conduce a la leucocitosis y aumento de sensibilidad a las infecciones como se ve en SLC35C1-CDG(CDG-IIc); causada por una deficiencia del transportador de PIB-fucosa (Fuc).
Oligosacáridos N-ligados todos proceden de un precursor común de lípidos vinculados oligosacárido (LLO), sintetizado en el ER un anclaje dolichol-phosphate (Dol-P). El maduro LLO se transfiere co-translationally a la secuencia consenso ASN los residuos de la proteína naciente y además es modificado por recortar y re-construir en el Golgi.
Las deficiencias en la genes involucrado en Glicosilación N-ligados constituyen el fondo molecular a la mayoría de los CDGs.
- Tipo I defectos involucran la síntesis y la transferencia de la LLO
- Defectos tipo II perjudicar el proceso de modificación de oligosacáridos unida a las proteínas.
Tipo I
| Descripción | Trastorno | Producto |
|---|---|---|
| La formación de la LLO se inicia por la síntesis de la polyisoprenyl Dolicol De farnesil, un precursor de colesterol biosíntesis. Este paso consiste en por lo menos tres genes, DHDDS (codificación dehydrodolichyl difosfato sintasa es un CIS-prenyl transferasa), DOLPP1 (un Pirofosfatasa) y SRD5A3, codificación de un reductasa completa la formación de Dolicol. | Recientemente, secuenciación exoma demostraron que las mutaciones en DHDDS causar un desorden con un fenotipo retiniana (Retinosis pigmentaria, un hallazgo común en pacientes CDG.[15] Además, el intermediario reductasa en este proceso (codificado por SRD5A3), es deficiente en SRD5A3-CDG (CDG-Iq).[16] |
|
| DOL entonces se activa a DOL-P mediante la acción de DOL quinasa En Membrana de ER. | Este proceso es defectuoso en DOLK-CDG (CDG-Im).[17] |

|
| Consecutivos N-acetilglucosamina (GlcNAc)- y mannosyltransferases utilizar la nucleótido donantes de azúcar UDP-GlcNAc y PIB-manosa (Hombre) para formar un Pirofosfato-siete vinculado glicanos estructura (Man5GlcNAc2-PP-Dol) de azúcar en la citoplasmática lado de la ER. | Algunos de estos pasos se han encontrado deficientes en los pacientes.
|
Man5GlcNAc2-PP-Dol |
| Luego se voltea la estructura de M5GlcNAc2 para el ER Lumen, mediante la acción de un "Flipasa" | Esto es deficiente en RFT1-CDG (CDG-In).[22] | |
| Por último, tres mannosyltransferases y tres glucosiltransferasas completar la estructura LLO Glc3Man9GlcNAc2-PP-Dol utilizando DOL-P-hombre y DOL-P-glucosa (Glc) como donantes. | Hay cinco defectos conocidos:
|
Glc3Man9GlcNAc2-PP-Dol |
| Una proteína con actividad hasta ahora desconocida, MPDU-1, es necesaria para la eficiente presentación de Dol-P-hombre y Dol-P-Glc. | Su deficiencia causa MPDU1-CDG (CDG-si).[28] | |
| La síntesis de PIB-hombre es crucial para la adecuada N-glicosilación, que sirve como sustrato de donantes para la formación de la estructura Man5GlcNAc2-P-Dol inicial y Dol-P-hombre. Síntesis del PIB-Man está vinculada a glucólisis vía la interconversión de fructosa-6-P y Hombre-6-P, catalizada por phosphomannose isomerase (PMI). | Este paso es deficiente en MPI-CDG (CDG-Ib),[29] ¿Cuál es el CDG solo tratable-subtipo. |

|
| Hombre-1-P se forma de hombre-6-P, catalizada por phosphomannomutase (PMM2), y el hombre-1-P sirve como sustrato en la síntesis del PIB-Man. | Mutaciones en PMM2 causa PMM2-CDG (CDG-Ia), el subtipo más común de CDG.[30] |

|
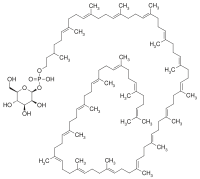
| DOL-P-hombre está formado por la acción de DOL-P-hombre sintasa, compuesta por tres subunidades; DPM1, DPM2, y DPM3. | Mutaciones en DPM1 causas DPM1-CDG (CDG-Ie). Curiosamente, las mutaciones en DPM2 (DPM2-CDG) y DPM3 (DPM3-CDG (CDG-Io))[31] provocar síndromes con un fenotipo muscular que se asemeja al-dystroglycanopathy, posiblemente debido a la falta de Dol-P-hombre necesario para O-mannosylation. |
|
| Los finales oligosacáridos 14mer Dol-PP-limite (Glc3Man9GlcNAc2-PP-Dol) se transfieren al consenso ASN los residuos en las proteínas aceptor en el lumen del re, catalizada por la oligosaccharyltransferase(OST). La banda sonora está compuesta por varias subunidades, incluyendo DDOST, TUSC3, MAGT1, KRTCAP2 y STT3a y - 3b. | Tres de estos genes ha demostrado para ser transformado en pacientes CDG, DDOST (DDOST-CDG (CDG-Ir)), TUSC3 hithero (TUSC3-CDG) y MAGT1 (MAGT1-CDG). |
Tipo II
La cadena LLO madura luego se transfiere a la cadena de la proteína creciente, un proceso catalizado por la oligosaccharyl transferasa Complejo (OST).
- Una vez transferida a la cadena de la proteína, el oligosacárido es recortada por glicosidasas específicos. Este proceso es vital desde el lectina acompañantes calnexin y calreticulina, en calidad de proteína, se unen a la estructura Glc1Man9GlcNAc y asegurar el correcto plegamiento. Falta de la primera (glucosidasaGCS1) causa CDG-IIb.
- Eliminación de los residuos Glc y el residuo de hombre primero ocurre en la sala de emergencias.
- La glicoproteína entonces viaja a la Golgi, donde se formó una multitud de diferentes estructuras con diferentes actividades biológicas.
- Manosidasa I crea una estructura de Man5GlcNAc2 en la proteína, pero nota que esta tiene una estructura diferente de la que hizo en LLO.
- A continuación, un residuo GlcNAc forma GlcNAc1Man5GlcNAc2, el sustrato para un-manosidasa II (sustanciasalucinógenas).
- sustanciasalucinógenas entonces elimina los residuos de dos hombre, creando el substrato para GlcNAc transferasa II, que agrega un GlcNAc a la segunda rama del hombre. Esta estructura sirve como sustrato para adicional galactosylation, fucosylation y Asimismo reacciones. Además, sustitución con más residuos GlcNAc puede producir moléculas tri - y tetra-antennary.
No todas las estructuras se modifican completamente, algunos permanecen estructuras tan alta-manosa, otros como los híbridos (una rama de hombre sin modificar y uno modificados), pero la mayoría se convierten en completamente modificada oligosacáridos tipo complejo.
Además de glucosidasa mutaciones han sido encontrados:
- en MGAT2, en GlcNAc transferasa II (CDG-IIa)
- en SLC35C1, el transportador del PIB-Fuc (CDG-IIc)
- en B4GALT1, un galactosyltransferase (CDG-IId)
- en COG7, el aparato de Golgi-7 oligoméricas conservados (CDG-IIe)
- en SLC35A1, el transportador de ácido (NeuAc) CMP-siálicos (CDG-IIf)
Sin embargo, el uso de > 100 genes en este proceso, probablemente significa que muchos más defectos deben ser encontrados.
Tratamiento
Ningún tratamiento está disponible para la mayoría de estos trastornos. Manosa la suplementación en su mayor parte, alivia los síntomas en el PMI-CDG (CDG-Ib)[32] Aunque la fibrosis hepática puede persistir.[33] Fucosa suplementación ha tenido un efecto parcial en algunos pacientes SLC35C1-CDG (CDG-CII o LAD-II).[34]
Véase también
- Errores innatos del metabolismo
- Deficiencia de la adherencia del leucocito
Referencias
- ^ Vanderschueren Jaeken, J.,-Lodeweyckx, M., Casaer, P., Snoeck, L., Corbeel, L., Eggermont, E. y Eeckels, r. (1980) Pediatr Res 14, 179
- ^ Jaeken, J. y Carchon, H. (1993) los síndromes de glicoproteína con deficiencia de carbohidratos: un resumen. J heredar Metab esquema 16, 813-20.
- ^ Jaeken, J., Schachter, H., Carchon, H., De Cock, P., Coddeville, B. y Spik, g. (1994) arco esquema niñez 71, 123-127
- ^ Niehues, R., Hasilik, M., Alton, G., Körner, C., Schiebe-Sukumar, M., Koch, H.G., Zimmer, K.P., Wu, R., Harms, E., Reiter, K., von Figura, K., congelación, H.H., Harms, H.K., Marquardt, T. deficiencia de carbohidrato glicoproteína síndrome tipo IB Phosphomannose isomerase deficiencia de y manosa terapia. Clin J. (1998). Invertir. 101, 1414-20.
- ^ Haeuptle, M.A. y Hennet, trastornos T. congénitos de la glicosilación: una actualización sobre defectos que afectan a la biosíntesis de oligosacáridos Dolicol-ligado. (2009) hum Mutat 30, 1628-41.
- ^ Necesito CA, Shashi V, Hitomi Y, et al (junio de 2012). "Aplicación clínica de la secuenciación del exoma en condiciones genéticas no diagnosticadas". J. med Genet. 49 (6): 353 – 61. Doi:10.1136/jmedgenet-2012-100819. PMC3375064. PMID22581936.
- ^ Enns GM, Shashi V, Bainbridge M, et al (marzo de 2014). "Mutaciones en NGLY1 causa un trastorno hereditario de la vía de degradación asociada a retículo endoplásmico". Genet. Med. Doi:10.1038/GIM.2014.22. PMID24651605.
- ^ Congelación de HH, EA Eklund, Ng BG, Patterson MC (mayo de 2012). "Neurobiología de la glicosilación heredado trastornos". Lanceta Neurol. 11 (5): 453 – 66. Doi:10.1016/S1474-4422 (12) 70040-6. PMID22516080.
- ^ Hennet Jaeken, J., T., Matthijs, G. y congelar, nomenclatura CDG H.H. (2009): la hora de un cambio. Biochim Biophys Acta. 1792, 825-6.
- ^ Wu, x., Steet, R.A., Bohorov, O., Bakker, J., Newell, J., Krieger, M., Spaapen, L., Kornfeld, S. y congelar, H.H. Mutation del gen complejo subunidad COG COG7 provoca un desorden congénito de letal. (2004) NAT med 10, 518-23.
- ^ Kornak U., E., A. Rivera, Reynders van Reeuwijk J., Fischer B., A. Rajab, Budde B., Nürnberg P., -1 #ARCL Debré-tipo Lefeber et al (2008). "Deteriorada glicosilación y cutis laxa causada por mutaciones en la vesicular H +-subunidad ATPasa ATP6V0A2". NAT Genet 40:: 4 32. Doi:10.1038/ng.2007.45.
- ^ Amberger J, C Bocchini, Hamosh A. (2011). "Una nueva cara y nuevos retos para Online herencia mendeliana en el hombre (OMIM ®). Hum Mutat. 32 (5): 564 – 7. Doi:10.1002/humu.21466. PMID21472891.
- ^ Jensen Kjaergaard S, H F Klie, Moller HU (2003). "Manifestaciones oftálmicas de desorden congénito del glycosylation tipo 1a". Genet oftálmico. 24 (2): 81 – 8. Doi:10.1076/opge.24.2.81.13994. PMID12789572.
- ^ El sol L, EA Eklund, Chung WK, Wang C, Cohen J, congelar HH (2005). "Desorden congénito del glycosylation id que presenta con hyperinsulinemic hipoglucemia y el islote hiperplasia de las células". J. Clin. Endocrinol. Metab. 90 (7): 4371 – 5. Doi:10.1210/JC.2005-0250. PMID15840742.
- ^ Züchner S, J Dallman, Wen R, Beecham G, Naj A, Farooq A, MA Kohli, Whitehead PL, Hulme W et al (2011). "La secuencia entera-exoma vincula una variante en DHDDS a retinosis pigmentaria". Soy J. Hum. Genet 88:: 201 – 6. Doi:10.1016/j.AJHG.2011.01.001.
- ^ Cantagrel, V., Lefeber, D.J., Ng, B.G., Guan, Z., Silhavy, J.L., cigüeñal, S.L., Lehle, L., Hombauer, H., Adamowicz, M., Swiezewska, E., De Brouwer, A.P., Blümel, P., Sykut-Cegielska,.J, Houliston, S., Swistun, D., Ali, B.R., Dobyns, W.B., Babovic-Vuksanovic, D., van Bokhoven, H., Wevers, R.A., Raetz, C.R., congelación, H.H., Morava, E., Al-prometen, L., Gleeson, J.G. SRD5A3 es necesaria para la conversión de Poliprenol a dolichol y es transformado en un desorden congénito del glycosylation. Célula (2010), 142, 203-17
- ^ C. Kranz, C. Jungeblut, J. Denecke, A. Erlekotte, C. Sohlbach, Debus V., Kehl, los daños E., Reith A. et al (2007). "Un defecto en la biosíntesis de dolicol fosfato provoca un nuevo desorden heredado con la muerte en la primera infancia". Soy J. Hum. Genet 80:: 433 – 40. Doi:10.1086/512130. PMC1821118. PMID17273964.
- ^ X. Wu, Rush J.S., Karaoglu D., Krasnewich D., Lubinsky M.S., C.J. Waechter, R. Gilmore, congelar H.H. (2003). "Deficiencia de UDP-GlcNAc:Dolichol fosfato de N-acetilglucosamina-1 fosfato transferasa (DPAGT1) provoca un nuevo desorden congénito del Glycosylation tipo Ij.". Zumbido. MUT. 22:: 144 – 50. Doi:10.1002/humu.10239.
- ^ C.E. Grubenmann, Frank C.G., Hülsmeier AJ, Schollen E., Matthijs G., E. Mayatepek, Berger por ejemplo, M. Aebi, Hennet T. et al (2004). "La deficiencia de la mannosylation primer paso en el camino de N-glicosilación causa desorden congénito del glycosylation tipo Ik.". Zumbido. Análizar Genet 13:: 535 – 42. Doi:10.1093/HMG/ddh050.
- ^ Thiel C., M. Schwarz, Peng J., M. Grzmil, M. Hasilik, Braulke T., Kohlschütter A., von Figura K., Lehle L. et al (2003). "Un nuevo tipo de trastornos congénitos de la glicosilación (CDG-Ii) ofrece nuevas perspectivas sobre los primeros pasos de la biosíntesis de oligosacárido dolichol-ligado". J Biol Chem 278:: 22498 – 505. Doi:10.1074/JBC.m302850200.
- ^ Corteza N, V Schmeiser, Thiel C, Absmanner B, Lübbehusen J, corvejones J, Apeshiotis N, Wilichowski E, Lehle L et al (2010). "Una severa enfermedad metabólica humana causada por deficiencia de la hALG11 endoplasmatic mannosyltransferase conduce al desorden congénito del glycosylation-Ip". Zumbido. Análizar Genet 19:: 1413 – 24. Doi:10.1093/HMG/ddq016.
- ^ Vleugels w., Haeuptle M.A., B.G. Ng, Michalski J.C., R. Battini, Dionisi-Vici C., M.D. Ludman, Jaeken j, Foulquier F. et al (2009). "Deficiencia de RFT1 en tres pacientes CDG novela". Zumbido. Mutat 30:: 1428 – 34. Doi:10.1002/humu.21085.
- ^ C. Körner, R. Knauer, Stephani U., T. Marquardt, Lehle L., von Figura K. (1999). "Tipo del síndrome de glicoproteínas deficientes en carbohidratos IV: deficiencia del dolichyl-P-hombre (5): GlcNAc 2-PP-dolichyl mannosyltransferase". EMBO J 18:: 6816 – 22. Doi:10.1093/emboj/18.23.6816.
- ^ Frank, C.G., Grubenmann, C.E., Eyaid, w., Berger, por ejemplo, Aebi, M. y Hennet, T. identificación y análisis funcional de un defecto en el gen humano ALG9: definición de desorden congénito del glycosylation tipo IL. (2004) soy J. Hum. Genet., 75, 146-50
- ^ Chantret I., T. Dupré, Delenda C., S. Bucher, Dancourt J., A. Barnier, Charollais A., D. Heron, Bader-Meunier B. et al (2002). "Trastornos congénitos de la glicosilación tipo Ig se define por una deficiencia en dolichyl-P-manosa: Man7GlcNAc2-PP-mannosyltransferase dolichyl". J Biol Chem 277:: 25815 – 22. Doi:10.1074/JBC.m203285200.
- ^ Körner, C., Knauer, R., Holzbach, U., Hanefeld, f el., Lehle, L. y von Figura, tipo de síndrome de deficiencia de K. (1998) carbohidrato glicoproteína V: deficiencia de dolichyl-P-Glc:Man9GlcNAc2-PP-glucosiltransferasa dolichyl. Proc. nacional Acad. Sci U S a, 95, 13200-5.
- ^ I. Chantret Dancourt J., T. Dupré, C. Delenda, Bucher S., S. Vuillaumier-Barrot, Ogier, de Baulny H., Peletan C. et al (2003). "Una deficiencia en dolichyl-P-glucosa: Glc1Man9GlcNAc2-PP-dolichyl alpha3-glucosiltransferasa define un nuevo subtipo de trastornos congénitos de la glicosilación". J Biol Chem 278:: 9962 – 71. Doi:10.1074/JBC.m211950200.
- ^ Kranz C. J. Denecke, M.A. Lehrman, Ray S., P. Kienz, Kreissel G., D. Sagi, J. Peter-Katalinic, congelar H.H. et al (2001). "Una mutación en el gene humano de MPDU1 causa desorden congénito del glycosylation tipo si (CDG-si)". J. Clin. Invertir 108:: 1613 – 9. Doi:10.1172/jci200113635.
- ^ Niehues R, Hasilik M, Alton G, Körner C, Schiebe-Sukumar M, Koch HG, Zimmer KP, Wu R, daños E, Reiter K, von Figura K, congelar HH, HK Harms, Marquardt T (1998). "Tipo IB Phosphomannose isomerase deficiencia y manosa terapia del síndrome de glicoproteína con deficiencia de carbohidratos". J. Clin. Invertir. 101 (7): 1414 – 20. Doi:10.1172/JCI2350. PMC508719. PMID9525984.
- ^ Matthijs G, E Schollen, perdón por Jaeken E, Veiga-Da-Cunha M, J, Cassiman JJ, Van Schaftingen E (1997). "Mutaciones en PMM2, un gene del phosphomannomutase en el cromosoma 16p13, de glicoproteína con deficiencia de carbohidrato tipo I (síndrome de Jaeken).". NAT Genet. 16 (1): 88-92. Doi:10.1038/ng0597-88. PMID9140401.
- ^ Lefeber DJ, Schönberger J, E Morava, Guillard M, Huyben KM, Verrijp K, Grafakou O, Evangeliou A, Preijers FW, Manta P, Yildiz J, Grünewald S, Spilioti M, van den Elzen C, D Klein, Hess D, Ashida H, Hofsteenge J, Maeda Y, van den Heuvel L, Lammens M, Lehle L, Wevers RA. (2009). "Deficiencia de la subunidad sintetasa Dol-P-hombre DPM3 puentes los trastornos congénitos de la glicosilación con el distroglicanopatías".. Soy J. Hum. Genet. 85 (1): 76-86. Doi:10.1016/j.AJHG.2009.06.006. PMC2706967. PMID19576565.
- ^ Mencionar, K., Lacaille, F., Valayannopoulos, V., Romano, S., Kuster, A., Cretz, M., Zaidan, H., Galmiche, L., Jaubert, f el., de Keyzer, Y., Seta, N. y de Lonlay, P. desarrollo de la enfermedad hepática a pesar del tratamiento de manosa en dos pacientes con Genet análizar CDG-IB (2008). Metab. 93, 40-3
- ^ Westphal, V., Kjaergaard, S., Davis, J.A., Peterson, S.M., Skovby, f el. y congelar, H.H. genéticos y metabólico análisis del primer adulto con el desorden congénito del glycosylation tipo Ib: resultado a largo plazo y los efectos de la suplementación de manosa. Genet PM (2001). Metab. 73, 77-85.
- ^ Eklund, E.A. y congelación, H.H. Los trastornos congénitos de la glicosilación: un grupo de síndromes múltiples facetas. (2006) NeuroRx 3, 254-63.
Enlaces externos
- Entrada de GeneReviews/NIH/NCBI/UW sobre Síndrome de glicoproteína con deficiencia de carbohidrato PMM2-CDG (CDG-Ia), tipo 1a; Desorden congénito del Glycosylation tipo 1a; Síndrome de Jaeken
- Entradas OMIM sobre Síndrome de glicoproteína con deficiencia de carbohidrato, tipo 1a; Desorden congénito del Glycosylation tipo 1a; Síndrome de Jaeken
- La red familiar de CDG
- Entrada de GeneReviews/NIH/NCBI/UW en trastornos congénitos de la glicosilación Resumen
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||